题目内容
16.下列说法正确的是( )| A. | 质子数为6,中子数为7的原子的元素符号可表示为${\;}_{6}^{13}$C | |
| B. | H2、SO2、CO三种气体都可用浓硫酸干燥 | |
| C. | 共价化合物溶于水,分子内共价键被破坏,单质溶于水,分子内共价键不被破坏 | |
| D. | 陶瓷、玻璃、水泥、大理石的主要成分都是硅酸盐 |
分析 A.元素符号的左上角为质量数;
B.所干燥的物质不能与干燥剂发生反应;
C.共价化合物溶于水,分子内共价键不一定被破坏;
D.玻璃、陶瓷和水泥是常用的硅酸盐产品.
解答 解:A.元素符号的左上角为质量数,质量数=质子数+中子数=7+6=13,故A正确;
B.H2、SO2、CO2三种气体和浓硫酸不反应,都可用浓硫酸干燥,故B正确;
C.共价化合物溶于水,分子内共价键不一定被破坏,如乙醇溶于水,故C错误;
D.大理石的主要成分是碳酸钙,故D错误.
故选AB.
点评 本题考查核素、浓硫酸作为干燥剂的性质分散系以及物质的成分等,题目难度不大,注意与浓硫酸反应的气体不能用浓硫酸干燥.

练习册系列答案
相关题目
4.加热NaHCO3和Na2CO3混合物20g,至质量不再变化为止,冷却后称量其固体质量是13.8g,则原混合物中Na2CO3的质量分数为( )
| A. | 84% | B. | 8.4% | C. | 1.6% | D. | 16% |
11.实验室中少量金属钠常常保存在( )
| A. | 水中 | B. | 煤油中 | C. | 密封容器中 | D. | 棕色瓶内 |
1.已知在常温下测得浓度均为0.1mol•L-1的下列四种溶液的pH如下表:
(1)用离子方程式表示NaClO溶液的pH=9.7的原因ClO-+H2O?HClO+OH-.
(2)根据盐溶液的pH,可知①Ka(HClO) ②Ka1(H2CO3) ③Ka(HF) ④Ka2(H2CO3)的大小顺序为③②①④.
(3)将少量CO2通入NaClO溶液中,写出该反应的离子方程式:CO2+H2O+ClO-=HClO+HCO3-.
(4)将CO2通入0.1mol•L-1的Na2CO3溶液中至中性,则溶液中2c(CO32-)+c(HCO3-)=0.2mol•L-1.
| 溶质 | NaHCO3 | Na2CO3 | NaF | NaClO |
| pH | 8.4 | 11.6 | 7.5 | 9.7 |
(2)根据盐溶液的pH,可知①Ka(HClO) ②Ka1(H2CO3) ③Ka(HF) ④Ka2(H2CO3)的大小顺序为③②①④.
(3)将少量CO2通入NaClO溶液中,写出该反应的离子方程式:CO2+H2O+ClO-=HClO+HCO3-.
(4)将CO2通入0.1mol•L-1的Na2CO3溶液中至中性,则溶液中2c(CO32-)+c(HCO3-)=0.2mol•L-1.
8.下列有关物质分类或归纳的说法中,正确的是( )
| A. | SO2、NO2和CO2都是污染性气体 | |
| B. | 熟石灰、铝热剂、盐酸都是混合物 | |
| C. | 煤的干馏、海水中提取碘的过程都包括化学变化 | |
| D. | A12O3、Cl2、CuSO4在熔融状态或溶于水时均能导电,都属电解质 |
5.容量瓶上需标有:①温度;②浓度;③容量;④刻度线;⑤酸式;⑥碱式 六项中的( )
| A. | ①③④ | B. | ③⑤⑥ | C. | ①②④ | D. | ②④⑥ |
6.下列实验装置能达到实验目的是( )
| A. |  进行喷泉实验 | B. |  加热熔融NaOH固体 | ||
| C. |  验证镁片与稀盐酸反应放热 | D. |  测定过氧化氢的纯度 |
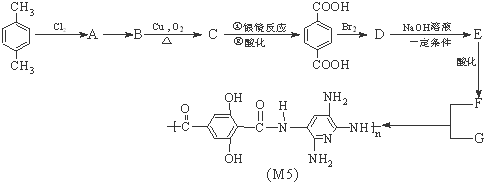
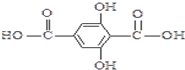 .
.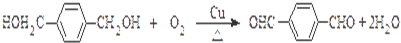 ,
,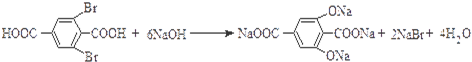 .
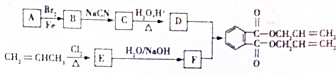
.
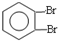 ,化合物E中所含的官能团名称为氯原子、碳碳双键.
,化合物E中所含的官能团名称为氯原子、碳碳双键.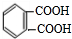 +2HOCH2CH=CH2$\stackrel{催化剂}{→}$
+2HOCH2CH=CH2$\stackrel{催化剂}{→}$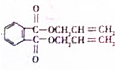 +2H2O,反应类型为酯化(取代)反应.
+2H2O,反应类型为酯化(取代)反应. (其中一种).
(其中一种).