题目内容
12.下列表述正确的是( )| A. | 氢氧根离子的电子式是 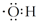 | |
| B. | 二氧化碳分子的比例模型是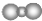 | |
| C. | 芳香烃的组成通式是CnH2n-6(n≥6) | |
| D. | 12C和14C的原子结构示意图均可表示为 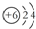 |
分析 A.氢氧根为阴离子,要用中括号括起来,并在右上角表明电荷数;
B.二氧化碳是直线形分子,同一周期元素中,原子直径随着原子序数的增大而减小;
C.CnH2n-6(n≥6)为苯及其同系物的通式,芳香烃没有通式;
D. 表示C元素原子结构示意图,与中子数无关.
表示C元素原子结构示意图,与中子数无关.
解答 解:A.氢氧根是带有1个负电荷的阴离子,要用中括号括起来,并在右上角表明电荷数,因氧原子最外层6个电子,氢原子最外层1个电子,则OH-的电子式为 ,故A错误;
,故A错误;
B.二氧化碳是直线形分子,同一周期元素中,原子直径随着原子序数的增大而减小,则二氧化碳分子正确的比例模型为: ,故B错误;
,故B错误;
C.含有苯环的烃都属于芳香烃,所以芳香烃没有通式,故C错误;
D.12C和14C的质子数都是6,其原子结构示意图相同,都可以表示为: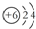 ,故D正确;
,故D正确;
故选D.
点评 本题考查了常见化学用语的判断,题目难度中等,注意掌握原子结构示意图、比例模型与球棍模型、电子式等化学用语的表示方法,明确球棍模型与比例模型、羟基与氢氧根离子的电子式的区别.

练习册系列答案
相关题目
5.下列微粒中,只有氧化性的是( )
①S2- ②Fe2+ ③Fe3+ ④S ⑤H+ ⑥Cu2+ ⑦Mg.
①S2- ②Fe2+ ③Fe3+ ④S ⑤H+ ⑥Cu2+ ⑦Mg.
| A. | ①⑦ | B. | ②④ | C. | ③⑤⑥ | D. | ②④⑤⑥ |
6.设NA为阿伏伽德常数的数值,下列说法正确的是( )
| A. | 18 g H2O含有10NA个质子 | |
| B. | 1 mol甲苯含有6NA个C-H键 | |
| C. | 标准状况下,22.4 L氨水含有NA个NH3分子 | |
| D. | 56 g铁片投入足量浓H2SO4中生成NA个SO2分子 |
4.可逆反应2NO2(g)?2NO(g)+O2(g)在体积不变的密闭容器中进行,达到化学平衡的标志是( )
| A. | 单位时间内生成n molO2的同时生成2n mol NO2 | |
| B. | 单位时间内生成n molO2的同时消耗2n mol NO2 | |
| C. | NO2的分解速率等于O2的形成速率 | |
| D. | 反应物和生成物的浓度相等 |
1.将pH=8,pH=10的两种强碱溶液以等体积比混合,求混合后所得溶液的pH值( )
| A. | 8.3 | B. | 8.7 | C. | 9 | D. | 9.7 |
19.下列离子方程式书写正确的是( )
| A. | 金属铝溶于氢氧化钠溶液中:Al+2OH-=AlO2-+H2↑ | |
| B. | 铜与稀硝酸反应:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O | |
| C. | 硫酸铵溶液与氢氧化钡溶液反应:NH4++OH-=NH3↑+H2O | |
| D. | 铁与稀硝酸反应:Fe+2H+=Fe2++H2↑ |
 B.
B. C.
C. D.
D.
 CH3COOC2H5+H2O.
CH3COOC2H5+H2O.