题目内容
17.下列离子方程式书写正确的是( )| A. | NaHCO3溶液中加入稀HNO3:CO${\;}_{3}^{2-}$+2H+═CO2↑+H2O | |
| B. | 碳酸钠溶液显碱性:CO${\;}_{3}^{2-}$+H2O?HCO${\;}_{3}^{-}$+OH- | |
| C. | Na2O2溶于水产生O2:Na2O2+H2O=2Na++2OH-+O2↑ | |
| D. | 碳酸氢钠溶液中滴入过量澄清石灰水:HCO${\;}_{3}^{-}$+OH-═CO${\;}_{3}^{2-}$+H2O |
分析 A.碳酸氢钠电离出碳酸氢根离子,碳酸氢根离子不能拆开;
B.碳酸根离子的水解分步进行,主要以第一步为主;
C.2mol过氧化钠与水反应生成1mol氧气,该反应不满足电子守恒;
D.石灰水过量,反应生成碳酸钙沉淀、氢氧化钠和水.
解答 解:A.NaHCO3溶液中加入稀HNO3,碳酸氢根离子不能拆开,正确的离子方程式为:HCO3-+H+═CO2↑+H2O,故A错误;
B.碳酸根离子水解溶液呈碱性,其水解主要以第一步为主,水解的离子方程式为:CO32-+H2O?HCO3-+OH-,故B正确;
C.Na2O2溶于水生成氢氧化钠和O2,正确的离子方程式为:2Na2O2+2H2O=4Na++4OH-+O2↑,故C错误;
D.向碳酸氢钠溶液中滴入过量澄清石灰水,反应生成碳酸钙沉淀、NaOH和水,正确的离子方程式为:Ca2++OH-+HCO3-=CaCO3↓+H2O,故D错误;
故选B.
点评 本题考查了离子方程式的判断,为高考的高频题,属于中等难度的试题,注意掌握离子方程式的书写原则,明确离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合守恒关系(如:质量守恒和电荷守恒等)等.

练习册系列答案
相关题目
7.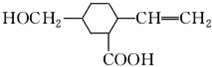 某有机物的结构如图所示,下列各项性质中,它不可能具有的是( )
某有机物的结构如图所示,下列各项性质中,它不可能具有的是( )
①可以燃烧 ②能使酸性KMnO4溶液褪色 ③能跟NaOH溶液反应 ④能发生酯化反应 ⑤能发生聚合反应 ⑥能发生水解反应 ⑦能发生取代反应.
 某有机物的结构如图所示,下列各项性质中,它不可能具有的是( )
某有机物的结构如图所示,下列各项性质中,它不可能具有的是( )①可以燃烧 ②能使酸性KMnO4溶液褪色 ③能跟NaOH溶液反应 ④能发生酯化反应 ⑤能发生聚合反应 ⑥能发生水解反应 ⑦能发生取代反应.
| A. | ①④ | B. | ⑤ | C. | ④⑥ | D. | ⑥ |
8.化学与生活密切相关,下列有关说法错误的是( )
| A. | 用灼烧的方法可以区分蚕丝和人造纤维 | |
| B. | 医用消毒酒精中乙醇的浓度为95% | |
| C. | 加热能杀死流感病毒是因为蛋白质受热变性 | |
| D. | 食用油反复加热会产生稠环芳香烃等有害物质 |
12.4℃下,把摩尔质量为Mg•mol-1的可溶性盐RCln(强电解质)Ag溶解在VmL水中,恰好形成该温度下的饱和溶液,密度为ρg•cm-3,下列关系式错误的是( )
| A. | 溶质的质量分数ω=$\frac{A}{(A+V)}×100%$ | |
| B. | 溶质的物质的量浓度c=$\frac{1000ρA}{(MA+MV)}mol•{L}^{-1}$ | |
| C. | 1mL该溶液中n(Cl-)=$\frac{nρAV}{M(A+V)}mol$ | |
| D. | 该温度下此盐的溶解度S=$\frac{100A}{V}g$ |
2.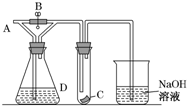 如图所示,A处通入Cl2,关闭B阀时,C处的红布看不到明显现象,开B阀后,C处红色布条逐渐褪色,则D瓶中装的不可能是( )
如图所示,A处通入Cl2,关闭B阀时,C处的红布看不到明显现象,开B阀后,C处红色布条逐渐褪色,则D瓶中装的不可能是( )
 如图所示,A处通入Cl2,关闭B阀时,C处的红布看不到明显现象,开B阀后,C处红色布条逐渐褪色,则D瓶中装的不可能是( )
如图所示,A处通入Cl2,关闭B阀时,C处的红布看不到明显现象,开B阀后,C处红色布条逐渐褪色,则D瓶中装的不可能是( )| A. | 浓H2SO4 | B. | NaOH溶液 | C. | Na2CO3溶液 | D. | 饱和NaCl溶液 |
9.A、B、C、D四个集气瓶中分别盛有Cl2、H2、HCl、HBr四种气体中的一种,A和B混合后,瓶壁上有红棕色小液滴出现;A和D混合后见光爆炸,则C瓶中盛的气体是( )
| A. | HCl | B. | Cl2 | C. | HBr | D. | H2 |
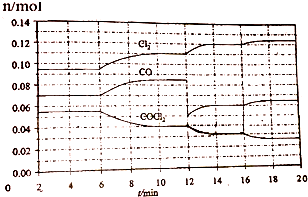
16.COCl2的分解反应为COCl2(g)?Cl2(g)+CO(g).将一定量COCl2(g)和Cl2(g)放入一密闭容器中,2min时达到平衡后,各物质的物质的量在不同条件下的变化情况如图所示.下列相关说法中不正确的是
( )
( )

| A. | 1min时以CO表示的逆反应速率小于3min时以CO表示的正反应速率 | |
| B. | 若在6min时改变的条件为升高温度,则反应的平衡常数K增大 | |
| C. | 12min时改变的条件可为减小CO的浓度,16min时改变的条件可为增大反应容器的体积 | |
| D. | 以CO表示在4~5min、10~11min和12~13min时平均反应速率为v(4~5)<v(10~11)<v(12~13) |
17.能将AlCl3、MgSO4、(NH4)2SO4、NH4Cl四种溶液区分开来的试剂是( )
| A. | AgNO3 | B. | BaCl2 | C. | NaOH | D. | Ba(OH)2 |
 有如图所示装置,为实现下列实验目的,其中Y端适合于作入口的是ABE.
有如图所示装置,为实现下列实验目的,其中Y端适合于作入口的是ABE.