题目内容
16.COCl2的分解反应为COCl2(g)?Cl2(g)+CO(g).将一定量COCl2(g)和Cl2(g)放入一密闭容器中,2min时达到平衡后,各物质的物质的量在不同条件下的变化情况如图所示.下列相关说法中不正确的是( )
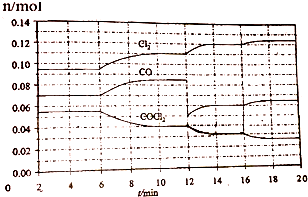
| A. | 1min时以CO表示的逆反应速率小于3min时以CO表示的正反应速率 | |
| B. | 若在6min时改变的条件为升高温度,则反应的平衡常数K增大 | |
| C. | 12min时改变的条件可为减小CO的浓度,16min时改变的条件可为增大反应容器的体积 | |
| D. | 以CO表示在4~5min、10~11min和12~13min时平均反应速率为v(4~5)<v(10~11)<v(12~13) |
分析 A.2min反应达到平衡状态,1min反应未达到平衡状态,达到平衡状态过程中CO浓度增大,逆反应速率增大;
B.6min升高温度,图象分析可知Cl2(g)、CO(g)物质的量增大,COCl2(g)物质的量减小,说明平衡正向进行;
C.12min时CO(g)物质的量突然减小,此时刻Cl2(g)、COCl2(g)物质的量不变,说明是减少CO的浓度,16min时改变条件Cl2(g)、CO(g)物质的量增大,COCl2(g)物质的量减小,说明平衡正向进行,改变的条件可能为减小压强;
D.根据化学反应速率的定义,可知反应在4~5 min和10~11 min处于平衡状态,CO的平均反应速率为0,12~13min时CO浓度减小反应速率减小.
解答 解:A.2min反应达到平衡状态,1min反应未达到平衡状态,达到平衡状态过程中CO浓度增大,逆反应速率增大,1min时以CO表示的逆反应速率小于3min时以CO表示的正反应速率,故A正确;
B.6min升高温度,图象分析可知Cl2(g)、CO(g)物质的量增大,COCl2(g)物质的量减小,说明平衡正向进行,平衡常数增大,故B正确;
C.12min时CO(g)物质的量突然减小,此时刻Cl2(g)、COCl2(g)物质的量不变,说明是减少CO的浓度,16min时改变条件Cl2(g)、CO(g)物质的量增大,COCl2(g)物质的量减小,说明平衡正向进行,改变的条件可能为减小压强,可为增大反应容器的体积,故C正确;
D.根据化学反应速率的定义,可知反应在4~5 min和10~11 min处于平衡状态,CO的平均反应速率为0,12~13min时CO浓度减小反应速率减小,v(4~5)=v(10~11)>v(12~13),故D错误;
故选D.
点评 本题考查化学平衡计算、平衡影响因素分析判断,为高频考点,明确外界条件对化学平衡影响、图中曲线含义及变化产生的原因等知识点是解本题关键,温度不变化学平衡常数不变,化学平衡常数与各物质浓度无关,题目难度中等.

 一本好题口算题卡系列答案
一本好题口算题卡系列答案| A. | 吸收471kJ能量 | B. | 放出479kJ能量 | C. | 吸收479kJ能量 | D. | 放出445kJ能量 |
| A. | NaHCO3溶液中加入稀HNO3:CO${\;}_{3}^{2-}$+2H+═CO2↑+H2O | |
| B. | 碳酸钠溶液显碱性:CO${\;}_{3}^{2-}$+H2O?HCO${\;}_{3}^{-}$+OH- | |
| C. | Na2O2溶于水产生O2:Na2O2+H2O=2Na++2OH-+O2↑ | |
| D. | 碳酸氢钠溶液中滴入过量澄清石灰水:HCO${\;}_{3}^{-}$+OH-═CO${\;}_{3}^{2-}$+H2O |
 许多含碳、含氢物质是重要的化工原料.
许多含碳、含氢物质是重要的化工原料.(1)某新型储氢合金(化学式为Mg17Al12)的储氧原理为Mg17Al12+17H2=17MgH2+12Al,此变化中氧化产物是MgH2(填化学式).
(2)C2O3是一种无色无味的气体,可溶于水生成草酸(H2C2O4),请写出它与足量NaOH溶液混合时反应的化学方程式:H2C2O4+2NaOH=Na2C2O4+2H2O.
(3)已知:①H2(g)+$\frac{1}{2}$O2(g)=H2O(g)△H1=-198kJ•mol-1
②CO(g)+$\frac{1}{2}$O2(g)=CO2(g)△H2
③CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H3=-846.3kJ•mol-1
| 化学键 | C≡O | O=O | C=O |
| 键能(kJ•mol-1) | 958.5 | 497 | 745 |
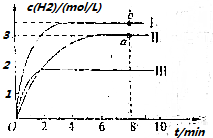
(4)向容积为2L的某恒容密闭容器中充入3molCH4、4molH2O,测出温度为T℃时,容器内H2物质的量浓度(mol/L)随时间的变化如图Ⅱ所示,图中Ⅰ、Ⅲ分别表示相对于Ⅱ仅改变反应条件后,c(H2)随时间的变化
①若曲线Ⅰ代表的是仅变化一种条件后的情况,则改变的条件可能是升温,a、b两点后用CO浓度变化表示的反应速率关系为a<b(填“>”“<”“=”).
②曲线Ⅱ对应反应的平衡常数为54,该温度下,若将等物质的量浓度的CH4、H2O、CO、H2混合在该容器中,则开始时H2的生成速率无法确定(填“>”“<”“=”或“无法确定”)H2的消耗速率.
③曲线Ⅲ相对于曲线Ⅱ改变的条件是b(填序号).
a.降低温度 b.使用催化剂、降低温度 c.充入氦气.
CH3CH2OH$→_{①}^{乙醇脱氢酶}$CH3CHO$→_{②}^{乙醛脱氢酶}$CH3COOH$→_{③}^{枸橼酸循环}$CO2+H2O
而双硫仑(
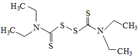 )会抑制肝脏中的乙醛脱氢酶,造成危害,严重的可能导致死亡.许多抗菌药(如:头孢)具有与双硫仑相似的作用,因此服用头孢后严禁饮酒.下列有关说法不正确的是( )
)会抑制肝脏中的乙醛脱氢酶,造成危害,严重的可能导致死亡.许多抗菌药(如:头孢)具有与双硫仑相似的作用,因此服用头孢后严禁饮酒.下列有关说法不正确的是( )| A. | “双硫仑”分子式为C10H12N2S4,在水中的溶解度较小 | |
| B. | 反应①②均属于氧化反应 | |
| C. | 一个人的酒量大小取决于体内上述两种酶的多少 | |
| D. | 乙醛是对人体有害的物质,含官能团名称为“醛基” |
| A. | 福尔马林、白酒、食醋 | B. | 冰醋酸、氯仿、乙醇钠 | ||
| C. | 无水酒精、甲苯、焦炉气 | D. | 乙烯、乙酸乙酯、煤 |

| A. | 分子中含有3种官能团 | |
| B. | 可与乙醇、乙酸、溴水发生反应,且反应类型相同 | |
| C. | 1mol分枝酸最多可与2molNaHCO3发生反应 | |
| D. | 可使溴的四氯化碳溶液、酸性高锰酸钾溶液褪色,且原理相同 |