题目内容
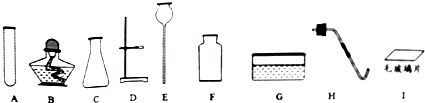
5. 有如图所示装置,为实现下列实验目的,其中Y端适合于作入口的是ABE.
有如图所示装置,为实现下列实验目的,其中Y端适合于作入口的是ABE.A.瓶内盛液体干燥剂,用以干燥气体
B.瓶内盛液体洗涤剂,用以除去某气体中的杂质
C.瓶内盛水,用以测量某难溶于水的气体的体积
D.瓶内贮存气体,加水时气体可被排出
E.收集密度比空气大的气体
F.收集密度比空气小的气体.
分析 Y端适合于作入口,可用于洗气、除杂、收集密度比空气密度大的气体,以此来解答.
解答 解:A.瓶内盛液体干燥剂,用以干燥气体,为洗气干燥装置,Y端适合于作入口,故选;
B.瓶内盛液体洗涤剂,用以除去某气体中的杂质,为除杂杂质,Y端适合于作入口,故选;
C.瓶内盛水,用以测量某难溶于水的气体的体积,应将水排出,则短端作气体入口,故不选;
D.瓶内贮存气体,加水时气体可被排出,则短端作气体入口,故不选;
E.收集密度比空气大的气体,Y端适合于作入口,故选;
F.收集密度比空气小的气体,则短端作气体入口,故不选;
故答案为:ABE.
点评 本题考查化学实验方案的评价,为高频考点,把握实验装置的作用、实验技能等为解答的关键,侧重分析与实验能力的考查,注意多用瓶在实验中的应用,题目难度不大.

练习册系列答案
 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案
相关题目
15.下列反应的离子方程式书写正确的是( )
| A. | 工业上用过量氨水吸收二氧化硫:NH3+SO2+H2O=NH4++HSO3- | |
| B. | 向氯化亚铁溶液中加入稀硝酸3Fe2++4H++NO3-=3Fe3++2H2O+NO↑ | |
| C. | 向(NH4)2SO4溶液中加入适量Ba(OH)2:Ba2++SO42-=BaSO4↓ | |
| D. | 硝酸铵与热氢氧化钠浓溶液反应:NH4++OH-=NH3•H2O |
16.已知断开1molH-H键,1mol O=O键和1molH-O键所吸收的能量分别为436kJ,497kJ,462kJ,则4g H2完全燃烧,该过程中的能量变化为( )
| A. | 吸收471kJ能量 | B. | 放出479kJ能量 | C. | 吸收479kJ能量 | D. | 放出445kJ能量 |
13.下列有关甲烷分子结构的说法中,错误的是( )
| A. | 甲烷分子中含有4个C-H共价键 | |
| B. | 甲烷分子中C-H共价键的夹角为109°28' | |
| C. | 甲烷是正四面体结构 | |
| D. | 甲烷是一种直线型分子 |
20.下列各组物质间的反应与反应类型不相符的是( )
| A. | 乙烯与溴水(加成反应) | |
| B. | 苯与浓硝酸(取代反应) | |
| C. | 乙醇与乙酸制乙酸乙酯(酯化反应) | |
| D. | 乙醇在铜、银等催化剂存在下与氧气(取代反应) |
17.下列离子方程式书写正确的是( )
| A. | NaHCO3溶液中加入稀HNO3:CO${\;}_{3}^{2-}$+2H+═CO2↑+H2O | |
| B. | 碳酸钠溶液显碱性:CO${\;}_{3}^{2-}$+H2O?HCO${\;}_{3}^{-}$+OH- | |
| C. | Na2O2溶于水产生O2:Na2O2+H2O=2Na++2OH-+O2↑ | |
| D. | 碳酸氢钠溶液中滴入过量澄清石灰水:HCO${\;}_{3}^{-}$+OH-═CO${\;}_{3}^{2-}$+H2O |
4. 许多含碳、含氢物质是重要的化工原料.
许多含碳、含氢物质是重要的化工原料.
(1)某新型储氢合金(化学式为Mg17Al12)的储氧原理为Mg17Al12+17H2=17MgH2+12Al,此变化中氧化产物是MgH2(填化学式).
(2)C2O3是一种无色无味的气体,可溶于水生成草酸(H2C2O4),请写出它与足量NaOH溶液混合时反应的化学方程式:H2C2O4+2NaOH=Na2C2O4+2H2O.
(3)已知:①H2(g)+$\frac{1}{2}$O2(g)=H2O(g)△H1=-198kJ•mol-1
②CO(g)+$\frac{1}{2}$O2(g)=CO2(g)△H2
③CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H3=-846.3kJ•mol-1
则CH4(g)+H2O(g)?CO(g)+3H2(g)的△H=30.6KJ/mol.
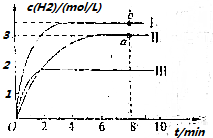
(4)向容积为2L的某恒容密闭容器中充入3molCH4、4molH2O,测出温度为T℃时,容器内H2物质的量浓度(mol/L)随时间的变化如图Ⅱ所示,图中Ⅰ、Ⅲ分别表示相对于Ⅱ仅改变反应条件后,c(H2)随时间的变化
①若曲线Ⅰ代表的是仅变化一种条件后的情况,则改变的条件可能是升温,a、b两点后用CO浓度变化表示的反应速率关系为a<b(填“>”“<”“=”).
②曲线Ⅱ对应反应的平衡常数为54,该温度下,若将等物质的量浓度的CH4、H2O、CO、H2混合在该容器中,则开始时H2的生成速率无法确定(填“>”“<”“=”或“无法确定”)H2的消耗速率.
③曲线Ⅲ相对于曲线Ⅱ改变的条件是b(填序号).
a.降低温度 b.使用催化剂、降低温度 c.充入氦气.
 许多含碳、含氢物质是重要的化工原料.
许多含碳、含氢物质是重要的化工原料.(1)某新型储氢合金(化学式为Mg17Al12)的储氧原理为Mg17Al12+17H2=17MgH2+12Al,此变化中氧化产物是MgH2(填化学式).
(2)C2O3是一种无色无味的气体,可溶于水生成草酸(H2C2O4),请写出它与足量NaOH溶液混合时反应的化学方程式:H2C2O4+2NaOH=Na2C2O4+2H2O.
(3)已知:①H2(g)+$\frac{1}{2}$O2(g)=H2O(g)△H1=-198kJ•mol-1
②CO(g)+$\frac{1}{2}$O2(g)=CO2(g)△H2
③CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H3=-846.3kJ•mol-1
| 化学键 | C≡O | O=O | C=O |
| 键能(kJ•mol-1) | 958.5 | 497 | 745 |
(4)向容积为2L的某恒容密闭容器中充入3molCH4、4molH2O,测出温度为T℃时,容器内H2物质的量浓度(mol/L)随时间的变化如图Ⅱ所示,图中Ⅰ、Ⅲ分别表示相对于Ⅱ仅改变反应条件后,c(H2)随时间的变化
①若曲线Ⅰ代表的是仅变化一种条件后的情况,则改变的条件可能是升温,a、b两点后用CO浓度变化表示的反应速率关系为a<b(填“>”“<”“=”).
②曲线Ⅱ对应反应的平衡常数为54,该温度下,若将等物质的量浓度的CH4、H2O、CO、H2混合在该容器中,则开始时H2的生成速率无法确定(填“>”“<”“=”或“无法确定”)H2的消耗速率.
③曲线Ⅲ相对于曲线Ⅱ改变的条件是b(填序号).
a.降低温度 b.使用催化剂、降低温度 c.充入氦气.
5.分枝酸可用于生化研究.其结构简式如图.下列关于分枝酸的叙述正确的是( )


| A. | 分子中含有3种官能团 | |
| B. | 可与乙醇、乙酸、溴水发生反应,且反应类型相同 | |
| C. | 1mol分枝酸最多可与2molNaHCO3发生反应 | |
| D. | 可使溴的四氯化碳溶液、酸性高锰酸钾溶液褪色,且原理相同 |