题目内容
16.对物质的量浓度相同的溶液的描述正确的是( )| A. | 溶液的质量相等 | |
| B. | 每升溶液中溶质的质量相等 | |
| C. | 相同体积的溶液,其溶质的物质的量相等 | |
| D. | 每升溶液中溶质的微粒数相等 |
分析 A.溶质浓度相同,溶液体积、密度不知不能确定溶液质量关系;
B.物质的量浓度是用单位体积的溶液中所含溶质物质的量表示,溶质摩尔质量不同;
C.依据n=cV分析等体积、等浓度的溶液中所含溶质物质的量相同;
D.对物质的量浓度相同的溶液,依据n=cV,每升溶液中溶质物质的量相同,溶质微粒数不一定相同.
解答 解:A.对物质的量浓度相同的溶液,溶液体积、溶液密度不同溶液质量不同,故A错误;
B.不同溶质摩尔质量不同,每升溶液中溶质的质量不相等,故B错误;
C.等体积、等浓度的溶液中所含溶质物质的量相同,故C正确;
D.根据n=cV,每升溶液中溶质物质的量相同,溶质微粒数不一定相同,如1mol/L的乙醇溶液和盐酸溶液中溶质微粒数不同,故D错误;
故选C.
点评 本题考查了物质的量浓度概念的理解应用,注意溶质质量、溶液质量、溶质物质的量和溶质微粒物质的量的比较,题目难度不大.

练习册系列答案
相关题目
6.下列说法正确的是( )
| A. | 在原电池中电子由正极流向负极 | |
| B. | 原电池负极和电解池阳极均发生氧化反应 | |
| C. | 在电解池中有氢气生成的电极可能是阳极 | |
| D. | 电镀时,镀层金属做阴极 |
4. 在体积为V L的恒容密闭容器中加入6mol CO和H2的混合气体,在不同条件下发生反应:CO(g)+2H2(g)═CH3OH(g).图甲表示有、无催化剂时反应的能量变化,图乙表示平衡时CH3OH的体积分数随起始n(CO):n(H2)的变化关系(图中I、II、III点均处于曲线上).下列叙述正确的是( )
在体积为V L的恒容密闭容器中加入6mol CO和H2的混合气体,在不同条件下发生反应:CO(g)+2H2(g)═CH3OH(g).图甲表示有、无催化剂时反应的能量变化,图乙表示平衡时CH3OH的体积分数随起始n(CO):n(H2)的变化关系(图中I、II、III点均处于曲线上).下列叙述正确的是( )
 在体积为V L的恒容密闭容器中加入6mol CO和H2的混合气体,在不同条件下发生反应:CO(g)+2H2(g)═CH3OH(g).图甲表示有、无催化剂时反应的能量变化,图乙表示平衡时CH3OH的体积分数随起始n(CO):n(H2)的变化关系(图中I、II、III点均处于曲线上).下列叙述正确的是( )
在体积为V L的恒容密闭容器中加入6mol CO和H2的混合气体,在不同条件下发生反应:CO(g)+2H2(g)═CH3OH(g).图甲表示有、无催化剂时反应的能量变化,图乙表示平衡时CH3OH的体积分数随起始n(CO):n(H2)的变化关系(图中I、II、III点均处于曲线上).下列叙述正确的是( )| A. | 该反应的热化学方程式为CO(g)+2H2(g)═CH3OH(g)△H=91 kJ•mol-1,曲线b表示使用了催化剂 | |
| B. | 反应速率:v (Ⅱ)<v (Ⅲ) | |
| C. | 平衡时CO的转化率:α(Ⅰ)<α(Ⅱ) | |
| D. | n(CO):n(H2)=0.5时,平衡时CH3OH的物质的量浓度:c(CH3OH,100℃)<c(CH3OH,200℃) |
11.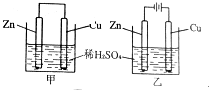 关于如图所示装置的叙述正确的是( )
关于如图所示装置的叙述正确的是( )
 关于如图所示装置的叙述正确的是( )
关于如图所示装置的叙述正确的是( )| A. | 甲乙装置中的铜片都作正极 | |
| B. | 甲乙装置中的溶液内的H+均在锌片上被氧化 | |
| C. | 甲乙装置中锌片上发生的反应都是还原反应 | |
| D. | 甲装置中铜片上有气泡生成,乙装置中的铜片质量减小 |
1.在国际环境问题中,一次性使用的聚苯乙烯材料带来的“白色污染”甚为突出.这种材料难以分解,处理麻烦.最近研究制出一种新型的材料能替代聚苯乙烯.它是由乳酸缩聚而生成的,该种材料可在乳酸菌作用下发生降解,下列关于聚乳酸的说法正确的是( )
| A. | 聚乳酸是一种纯净物 | B. | 其聚合方式与聚苯乙烯相似 | ||
| C. | 其单体为  | D. | 聚乳酸是一种线型高分子材料 |
8.下列实验的现象与对应的结论均正确的是( )
| 选项 | 操 作 | 现 象 | 结 论 |
| A | 向溶液X中滴加NaOH浓溶液,加热,将湿润的红色石蕊试纸置于试管口 | 试纸变蓝 | 溶液X中有NH4+ |
| B | 将过量过氧化钠固体投入紫色石蕊试液中 | 溶液变成红色 | 过氧化钠与水反应生成氢氧化钠,溶液呈碱性 |
| C | 将水蒸气通过灼热的铁粉 | 粉末变红 | 铁与水在高温下发生反应 |
| D | 常温下,将铜放入浓硫酸中 | 无明显变化 | 铜在冷的浓硫酸中钝化 |
| A. | A | B. | B | C. | C | D. | D |

 +H2O
+H2O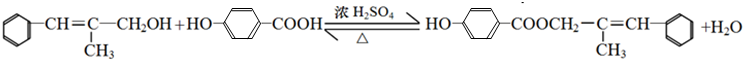
 .
.