题目内容
8.下列实验的现象与对应的结论均正确的是( )| 选项 | 操 作 | 现 象 | 结 论 |
| A | 向溶液X中滴加NaOH浓溶液,加热,将湿润的红色石蕊试纸置于试管口 | 试纸变蓝 | 溶液X中有NH4+ |
| B | 将过量过氧化钠固体投入紫色石蕊试液中 | 溶液变成红色 | 过氧化钠与水反应生成氢氧化钠,溶液呈碱性 |
| C | 将水蒸气通过灼热的铁粉 | 粉末变红 | 铁与水在高温下发生反应 |
| D | 常温下,将铜放入浓硫酸中 | 无明显变化 | 铜在冷的浓硫酸中钝化 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.润的红色石蕊试变蓝,说明反应生成的是氨气,则原溶液中含有铵根离子;
B.过氧化钠具有强氧化性,能使有色物质褪色;
C.反应生成四氧化三铁和氢气;
D.水蒸气与铁粉反应生成四氧化三铁,四氧化三铁为黑色固体.
解答 解:A.向溶液X中滴加NaOH浓溶液,加热,将湿润的红色石蕊试纸置于试管口,若试纸变蓝,说明生成气体为氨气,则溶液X中含有NH4+,故A正确;
B.过氧化钠具有强氧化性,能使有色物质褪色,过氧化钠和水反应生成NaOH导致溶液呈碱性,紫色石蕊试液遇碱变蓝色,所以溶液先变蓝色后褪色,故B错误;
C.反应生成四氧化三铁和氢气,粉末不会变红,现象不合理,故C错误;
D.将水蒸气通过灼热的铁粉,生成的是黑色的四氧化三铁,该实验现象不合理,故D错误;
故选A.
点评 本题考查化学实验方案的评价,为高频考点,题目难度中等,涉及氨气的制备及检验、铁的性质、过氧化钠的性质等知识,侧重实验操作及实验原理的考查,注意实验方案的可行性、操作性及评价性的分析.

练习册系列答案
 互动英语系列答案
互动英语系列答案 名牌学校分层周周测系列答案
名牌学校分层周周测系列答案 黄冈海淀全程培优测试卷系列答案
黄冈海淀全程培优测试卷系列答案
相关题目
19.下列金属冶炼原理的化学反应中,属于置换反应的是( )
| A. | 电解熔融的氯化钠制取钠 | B. | 用一氧化碳还原氧化铁制取铁 | ||
| C. | 加热分解氧化汞制取汞 | D. | 铁与硫酸铜溶液反应制取铜 |
16.对物质的量浓度相同的溶液的描述正确的是( )
| A. | 溶液的质量相等 | |
| B. | 每升溶液中溶质的质量相等 | |
| C. | 相同体积的溶液,其溶质的物质的量相等 | |
| D. | 每升溶液中溶质的微粒数相等 |
13.用下列实验装置进行实验,能达到相应实验目的是( )
| A. | 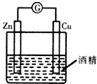 形成原电池 | B. | 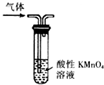 除去乙烯中混有的SO2 | ||
| C. | 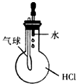 验证HCl气体在水中的溶解性 | D. | 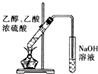 实验室制取乙酸乙酯 |
20.在一个恒容绝热的密闭容器中,发生可逆反应:M(?)+2N(g)?P(g)+Q(g) 该反应为吸热反应,已知M的状态未知,则下列描述一定达到平衡的标志是( )
①当物质M、N、P的体积分数比为 1:1:1时 ②混合气体的密度不变时
③体系的温度不变时 ④反应速率2v (N)正=v (Q)逆时
⑤体系的压强不变时 ⑥气体的平均相对分子质量不变时.
①当物质M、N、P的体积分数比为 1:1:1时 ②混合气体的密度不变时
③体系的温度不变时 ④反应速率2v (N)正=v (Q)逆时
⑤体系的压强不变时 ⑥气体的平均相对分子质量不变时.
| A. | ①③④ | B. | ③⑤⑥ | C. | ②③⑥ | D. | ③④⑤ |
17.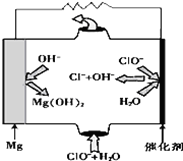 镁--次氯酸盐燃料电池具有比能量高、安全方便等优点,该电池主要工作原理如图所示,其正极反应为:ClO-+H2O+2e-═Cl-+2OH-,关于该电池的叙述正确的是( )
镁--次氯酸盐燃料电池具有比能量高、安全方便等优点,该电池主要工作原理如图所示,其正极反应为:ClO-+H2O+2e-═Cl-+2OH-,关于该电池的叙述正确的是( )
 镁--次氯酸盐燃料电池具有比能量高、安全方便等优点,该电池主要工作原理如图所示,其正极反应为:ClO-+H2O+2e-═Cl-+2OH-,关于该电池的叙述正确的是( )
镁--次氯酸盐燃料电池具有比能量高、安全方便等优点,该电池主要工作原理如图所示,其正极反应为:ClO-+H2O+2e-═Cl-+2OH-,关于该电池的叙述正确的是( )| A. | 该电池中镁为负极,发生还原反应 | |
| B. | 该电池的总反应为:Mg+ClO-+H2O═Mg(OH)2↓+Cl- | |
| C. | 电池工作时,正极周围溶液的碱性将不断减弱 | |
| D. | 电池工作时,OH-向正极移动 |
18.铜、铬都是用途广泛的金属.工业上利用电镀污泥(主要含有Fe2O3、CuO、Cr2O3及部分难溶杂质)回收金属铜和铬的流程如图1:
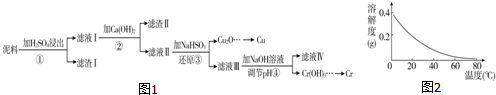
已知:部分物质沉淀的pH如表:
CaSO4的溶解度曲线如图2.
请回答下列问题:
(1)滤液Ⅰ中所含溶质主要有Fe2(SO4)3、Cr2(SO4)3、CuSO4(填化学式).
(2)第②步操作中,先加入Ca(OH)2调节溶液的pH,调节范围为3.2≤pH<4.3,然后将浊液加热至80℃趁热过滤,所得滤渣Ⅱ的成分为Fe(OH)3、CaSO4.
(3)第③步操作中,发现除了生成砖红色沉淀外,还产生了无色刺激性气味的气体.写出该步骤中发生反应的离子方程式2H2O+HSO3-+2Cu2+=Cu2O↓+SO42-+5H+、HSO3-+H+=SO2↑+H2O.
(4)当离子浓度≤1×10-5 mol•L-1时,可以认为离子沉淀完全.第④步操作中,若要使Cr3+完全沉淀,则室温下溶液中a的最小值为5.6.已知:Ksp[Cr(OH)3]=6.3×10-31,$\root{3}{64}$≈4.0;lg 4=0.6.
(5)Cr(OH)3受热分解为Cr2O3,用铝热法可以冶炼金属铬.写出铝热法炼铬的化学方程式Cr2O3+2Al$\frac{\underline{\;高温\;}}{\;}$Al2O3+2Cr.

已知:部分物质沉淀的pH如表:
| Fe3+ | Cu2+ | Cr3+ | |
| 开始沉淀pH | 2.1 | 4.7 | 4.3 |
| 完全沉淀pH | 3.2 | 6.7 | a |
请回答下列问题:
(1)滤液Ⅰ中所含溶质主要有Fe2(SO4)3、Cr2(SO4)3、CuSO4(填化学式).
(2)第②步操作中,先加入Ca(OH)2调节溶液的pH,调节范围为3.2≤pH<4.3,然后将浊液加热至80℃趁热过滤,所得滤渣Ⅱ的成分为Fe(OH)3、CaSO4.
(3)第③步操作中,发现除了生成砖红色沉淀外,还产生了无色刺激性气味的气体.写出该步骤中发生反应的离子方程式2H2O+HSO3-+2Cu2+=Cu2O↓+SO42-+5H+、HSO3-+H+=SO2↑+H2O.
(4)当离子浓度≤1×10-5 mol•L-1时,可以认为离子沉淀完全.第④步操作中,若要使Cr3+完全沉淀,则室温下溶液中a的最小值为5.6.已知:Ksp[Cr(OH)3]=6.3×10-31,$\root{3}{64}$≈4.0;lg 4=0.6.
(5)Cr(OH)3受热分解为Cr2O3,用铝热法可以冶炼金属铬.写出铝热法炼铬的化学方程式Cr2O3+2Al$\frac{\underline{\;高温\;}}{\;}$Al2O3+2Cr.