题目内容
6.下列说法正确的是( )| A. | 在原电池中电子由正极流向负极 | |
| B. | 原电池负极和电解池阳极均发生氧化反应 | |
| C. | 在电解池中有氢气生成的电极可能是阳极 | |
| D. | 电镀时,镀层金属做阴极 |
分析 A、在原电池中电子由负极流向正极;
B、原电池负极和电解池阳极均发生氧化反应;
C、在电解池中有氢气是氢离子在阴极放电生成氢气;
D、电镀时,镀层金属做阳极,发生氧化反应.
解答 解:A、在原电池中电子由负极流向正极,而电流由正极流向负极,故A错误;
B、原电池负极和电解池阳极均发生氧化反应,故B正确;
C、在电解池中有氢气是氢离子在阴极放电生成氢气,而不是阳极,故C错误;
D、电镀时,镀层金属做阳极,发生氧化反应,镀件做阴极,故D错误;
故选B.
点评 本题考查了电化学的知识,难度不大,会判断电子在外电路的流向及溶液中阴阳离子的移动方向,学生要清楚原电池负极和电解池阳极均发生氧化反应.

练习册系列答案
 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案
相关题目
16.下列除去杂质的方法正确的是( )
①除去乙烷中少量的乙烯:通入氢气让乙烯充分反应;
②除去乙酸乙酯中少量的乙酸:用饱和碳酸钠溶液洗涤、分液、干燥、蒸馏;
③除去CO2中少量的SO2:气体通过盛饱和碳酸钠溶液的洗气瓶;
④除去乙醇中少量的乙酸:加足量生石灰,蒸馏.
①除去乙烷中少量的乙烯:通入氢气让乙烯充分反应;
②除去乙酸乙酯中少量的乙酸:用饱和碳酸钠溶液洗涤、分液、干燥、蒸馏;
③除去CO2中少量的SO2:气体通过盛饱和碳酸钠溶液的洗气瓶;
④除去乙醇中少量的乙酸:加足量生石灰,蒸馏.
| A. | ①② | B. | ②④ | C. | ③④ | D. | ②③ |
17.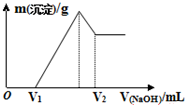 将0.1mol的镁、铝混合物溶于100mL 2mol/L H2SO4溶液中,然后再滴加1mol/L NaOH溶液.在滴加NaOH溶液的过程中,沉淀质量m随加入NaOH溶液的体积V变化如图所示.下列说法不正确的是( )
将0.1mol的镁、铝混合物溶于100mL 2mol/L H2SO4溶液中,然后再滴加1mol/L NaOH溶液.在滴加NaOH溶液的过程中,沉淀质量m随加入NaOH溶液的体积V变化如图所示.下列说法不正确的是( )
 将0.1mol的镁、铝混合物溶于100mL 2mol/L H2SO4溶液中,然后再滴加1mol/L NaOH溶液.在滴加NaOH溶液的过程中,沉淀质量m随加入NaOH溶液的体积V变化如图所示.下列说法不正确的是( )
将0.1mol的镁、铝混合物溶于100mL 2mol/L H2SO4溶液中,然后再滴加1mol/L NaOH溶液.在滴加NaOH溶液的过程中,沉淀质量m随加入NaOH溶液的体积V变化如图所示.下列说法不正确的是( )| A. | O~V1发生反应的离子方程式为:H++OH-═H2O | |
| B. | 当V1=160mL时,V2的体积为360mL | |
| C. | 当V1=160mL时,金属混合物中镁的质量为1.44g | |
| D. | 当Mg2+、Al3+刚好沉淀完全,则滴入的NaOH溶液的体积为400mL |
14.下列说法正确的是( )
| A. | 摩尔是一种物理量 | B. | Cl2的摩尔质量是71g | ||
| C. | 1molO2的体积是22.4L | D. | 36gH2O含有的分子数为2NA |
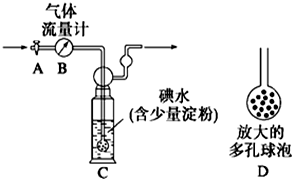
1. 欲用图装置进行实验,用以比较苯酚、盐酸、碳酸的酸性,图中标示的A、B、C三种药品(或试剂)依次是( )
欲用图装置进行实验,用以比较苯酚、盐酸、碳酸的酸性,图中标示的A、B、C三种药品(或试剂)依次是( )
 欲用图装置进行实验,用以比较苯酚、盐酸、碳酸的酸性,图中标示的A、B、C三种药品(或试剂)依次是( )
欲用图装置进行实验,用以比较苯酚、盐酸、碳酸的酸性,图中标示的A、B、C三种药品(或试剂)依次是( )| A. | 盐酸、碳酸、苯酚 | B. | 盐酸、碳酸钠、苯酚钠 | ||
| C. | 盐酸、碳酸钠、苯酚 | D. | 氯化钠、碳酸钠、苯酚钠 |
15.下列有关阿伏加德罗常数(NA)的说法错误的是( )
| A. | 44 g CO2所含的原子数为NA | |
| B. | 0.5 mol H2O含有的原子数目为1.5NA | |
| C. | 1 mol H2O含有的H2O分子数目为NA | |
| D. | 0.5NA个O2的物质的量是0.5 mol |
16.对物质的量浓度相同的溶液的描述正确的是( )
| A. | 溶液的质量相等 | |
| B. | 每升溶液中溶质的质量相等 | |
| C. | 相同体积的溶液,其溶质的物质的量相等 | |
| D. | 每升溶液中溶质的微粒数相等 |