题目内容
3.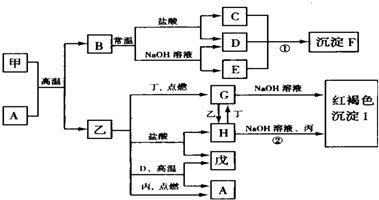 已知在一定条件下可实现如图所示物质之间的变化,其中甲、乙为金属单质,丙、丁、戊为非金属单质,B为氧化物.
已知在一定条件下可实现如图所示物质之间的变化,其中甲、乙为金属单质,丙、丁、戊为非金属单质,B为氧化物.请填写下列空白:
(1)物质A的化学式是Fe3O4,甲的原子结构示意图分别是
 ;
;(2)反应①的离子方程式是3AlO2-+Al3++6H2O═4Al(OH)3↓.
(3)反应②的化学方程式是(可以分步书写)FeCl2+2NaOH═Fe(OH)2↓+2NaCl、4Fe(OH)2+O2+2H2O═4Fe(OH)3.
乙和D在高温条件下反应生成1molA时转移电子的物质的量为8mol.
(4)若要除去H溶液中的G杂质,请简述方案:加入过量铁粉并过滤,该过程的离子反应方程式为:Fe+2Fe3+═3Fe2+.
分析 金属甲与A反应生成氧化物B与金属单质乙,而氧化物B既能与盐酸又能与NaOH溶液反应,则A为Al,B为Al2O3,C为AlCl3,E为NaAlO2,D为H2O,F为Al(OH)3.金属乙与非金属单质丁反应得到G,乙与盐酸反应生成H,H与丁反应得到G,G与NaOH溶液反应得到红褐色沉淀I,则乙为Fe,丁为Cl2,G为FeCl3,H为FeCl2,I为Fe(OH)3,乙(Fe)与D(H2O)反应生成的A为Fe3O4,戊为H2,乙与丙反应得到A,则丙为O2.
解答 解:金属甲与A反应生成氧化物B与金属单质乙,而氧化物B既能与盐酸又能与NaOH溶液反应,则A为Al,B为Al2O3,C为AlCl3,E为NaAlO2,D为H2O,F为Al(OH)3.金属乙与非金属单质丁反应得到G,乙与盐酸反应生成H,H与丁反应得到G,G与NaOH溶液反应得到红褐色沉淀I,则乙为Fe,丁为Cl2,G为FeCl3,H为FeCl2,I为Fe(OH)3,乙(Fe)与D(H2O)反应生成的A为Fe3O4,戊为H2,乙与丙反应得到A,则丙为O2.
(1)物质A的化学式是Fe3O4,甲为Al,原子结构示意图是 ,
,
故答案为:Fe3O4; ;
;
(2)反应①的离子方程式是:3AlO2-+Al3++6H2O═4Al(OH)3↓,
故答案为:3AlO2-+Al3++6H2O═4Al(OH)3↓;
(3)反应②的化学方程式是(可以分步书写):FeCl2+2NaOH═Fe(OH)2↓+2NaCl、4Fe(OH)2+O2+2H2O═4Fe(OH)3,
乙和D在高温条件下反应方程式为:3Fe+4H2O$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2,生成1molFe3O4时转移电子的物质的量为8mol,
故答案为:FeCl2+2NaOH═Fe(OH)2↓+2NaCl、4Fe(OH)2+O2+2H2O═4Fe(OH)3;8;
(4)要除去FeCl2溶液中的FeCl3杂质,可以向FeCl2溶液中加入过量铁粉并过滤,该过程的离子反应方程式为:Fe+2Fe3+═3Fe2+,
故答案为:加入过量铁粉并过滤;Fe+2Fe3+═3Fe2+.
点评 本题考查无机物的推断,物质的颜色、转化中特殊反应等是推断突破口,需要学生熟练掌握元素化合物性质,难度中等.

 名校课堂系列答案
名校课堂系列答案| A. | 在化工厂周围种绿色植物 | |
| B. | 不得排放废水、废气、废渣 | |
| C. | 以绿色植物为原料,用生物催化剂进行化工生产,且原子利用率达到100% | |
| D. | 尽可能减少对环境的污染 |
| A. | 已烷 | B. | 已烯 | C. | 1,2-二溴丙烷 | D. | 戊醇 |
| A. | 油脂在碱性条件下发生皂化反应 | |
| B. | 淀粉水解的最终产物是葡萄糖 | |
| C. | 葡萄糖、蔗糖、麦芽糖都能发生银镜反应 | |
| D. | 蛋白质水解的最终产物都是氨基酸 |
| A. | ${\;}_{6}^{14}$C和${\;}_{6}^{12}$C是同一种核素 | |
| B. | 红磷和白磷互为同素异形体 | |
| C. | CH3COOCH2CH3和CH3CH2COOCH3是不同物质 | |
| D. | CH3CH2OH可看成是由-C2H5和-OH组成 |

| A. | 装置①可用于实验室制取乙酸乙酯 | |
| B. | 装置②可观察铁的吸氧腐蚀 | |
| C. | 装置③中X为四氯化碳,该装置可用于吸收氨气或氯化氢 | |
| D. | 装置④为实验室蒸馏石油装置 |
| A. | 相同温度时,100mL0.01mol/L的醋酸溶液与10mL0.1mol/L的醋酸溶液相比较,H+的物质的量前者等于后者 | |
| B. | 在稀溶液中,H+(aq)+OH-(aq)═H2O(l)△H=-57.3KJ/mol,若将含1mol CH3COOH的稀溶液与含1molNaOH的稀溶液混合,放出的热量小于57.3KJ | |
| C. | 反应2Mg(s)+CO2(g)═C(s)+2MgO(s)能自发进行,则该反应的△H>0 | |
| D. | N2(g)+3H2(g)═2NH3(g)△H<0.其他条件不变时升高温度,反应速率和氢气的平衡转化率均增大 |

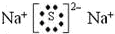 .
.