题目内容
化学无处不在,下列与化学有关的说法不正确的是( )
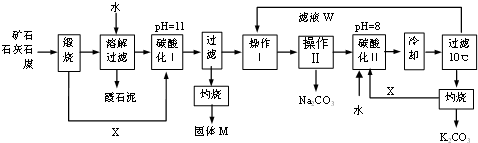
| A、侯氏制碱法的工艺过程中应用了物质溶解度的差异 |
| B、硅胶可以除去氯气中的水蒸气 |
| C、明矾净水属于物理变化 |
| D、黑火药由硫黄、硝石、木炭三种物质按一定比例混合制成 |
考点:物理变化与化学变化的区别与联系,纯碱工业(侯氏制碱法)
专题:
分析:A.侯氏制碱法是将CO2、NH3通入饱和NaCl溶液中,由于NaHCO3溶解度小于Na2CO3,故NaHCO3在溶液中析出;
B.硅胶能做干燥剂;
C.铝离子水解生成氢氧化铝胶体和氢离子;
D.硫磺、硝石、木炭三种物质比例为1:2:3.
B.硅胶能做干燥剂;
C.铝离子水解生成氢氧化铝胶体和氢离子;
D.硫磺、硝石、木炭三种物质比例为1:2:3.
解答:
解:A.侯氏制碱法是将CO2、NH3通入饱和NaCl溶液中,发生以下反应:NH3+CO2+H2O=NH4HCO3;NH4HCO3+NaCl=NH4Cl+NaHCO3↓,其中NaHCO3溶解度最小,故有NaHCO3的晶体析出,故A正确;
B.硅胶能做干燥剂,可以除去氯气中的水蒸气,故B正确;
C.铝离子水解生成氢氧化铝胶体和氢离子,氢氧化铝胶体具有吸附性,吸附水中的悬浮物,故C错误;
D.制备黑火药的原料为S、KNO3、C,三者比例为1:2:3,故D正确;
故选C.
B.硅胶能做干燥剂,可以除去氯气中的水蒸气,故B正确;
C.铝离子水解生成氢氧化铝胶体和氢离子,氢氧化铝胶体具有吸附性,吸附水中的悬浮物,故C错误;
D.制备黑火药的原料为S、KNO3、C,三者比例为1:2:3,故D正确;
故选C.
点评:本题考查物理变化与化学变化、侯氏制碱法原理等知识,试题较为综合,与人们日常生活紧密结合,均为最基本化学常识,选项C为易错点,关键在于判断变化过程中是否有新物质生成.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
用NA表示阿伏加德罗常数,下列物质中所含分子数目最多的是( )
| A、含NA个分子的氮气 |
| B、标准状况下3.36L甲烷 |
| C、5.4 g水(水的摩尔质量为18g?mol-1) |
| D、0.4mol三氧化硫 |
下列溶液中离子浓度的关系一定正确的是( )
| A、NH4Cl溶液中:c(Cl-)+c(H+)=c(NH4+)+c(OH-)+2c(NH3.H2O) |
| B、Na2CO3和NaHCO3溶液中:c(Na+)+c(H+)=c(OH-)+c(HCO3-)+c(CO32-) |
| C、等物质的量的一元弱酸HX与其钾盐KX的混合溶液中:2c(K+)=c(X-)+c(HX)+c(H+) |
| D、pH=3的一元酸HX和pH=11的一元碱MOH等体积混合:c(M+)=c(X-)>c(H+)=c(OH-) |
下列说法正确的是( )
| A、s能级的能量总是小于p能级的能量 |
| B、2s的电子云比1s的电子云大,说明2s的电子云中的电子比1s的多 |
| C、当电子排布在同一能级的不同轨道时,电子总是先占满1个轨道,然后再占据其他原子轨道 |
| D、nf能级中最多可容纳14个电子 |
臭名昭著的三聚氰酸[C3N3(OH)3]却可用于消除汽车尾气中的NO2.其反应原理为:
C3N3(OH)3
3HNCO; 8HNCO+6NO2
7N2+8CO2+4H2O下列说法正确的是( )
C3N3(OH)3
| ||
| ||
| A、C3N3(OH)3与HNCO为同一物质 |
| B、HNCO是一种很强的氧化剂 |
| C、1molNO2在反应中转移的电子为4mol |
| D、CO2既不是氧化产物,也不是还原产物 |