题目内容
把下列四种碳酸氢钠溶液分别加入四个盛有10mL 2mol?L-1盐酸的烧杯中,均加水稀释到50mL,此时碳酸氢钠和盐酸反应,其中反应开始时速率最大的是( )
| A、10℃20 mL 3 mol?L-1的碳酸氢钠溶液 |
| B、20℃30 mL 2 mol?L-1的碳酸氢钠溶液 |
| C、20℃10 mL 4 mol?L-1的碳酸氢钠溶液 |
| D、10℃20 mL 2 mol?L-1的碳酸氢钠溶液 |
考点:化学反应速率的影响因素
专题:化学反应速率专题
分析:均加水稀释到50mL,后来溶液的总体积相同,则选项中物质的量越大,温度越高,反应速率越大,以此来解答.
解答:
解:B、C中温度大于A、D中温度,则B、C中反应速率大,
B中碳酸氢钠的物质的量为0.03L×2mol/L=0.06mol,
C中碳酸氢钠的物质的量为0.01L×4mol/L=0.04mol,
显然B中浓度大,反应速率快,
故选B.
B中碳酸氢钠的物质的量为0.03L×2mol/L=0.06mol,
C中碳酸氢钠的物质的量为0.01L×4mol/L=0.04mol,
显然B中浓度大,反应速率快,
故选B.
点评:本题考查化学反应速率的影响因素,为高频考点,侧重于学生的分析能力和计算能力的考查,注意先比较温度再比较浓度为解答该题的关键,题目难度不大.

练习册系列答案
相关题目
下列分子的立体结构,其中属于直线型分子的是( )
| A、H2O |
| B、CO2 |
| C、C2H4 |
| D、P4 |
下列描述中,不符合生产实际的是( )
| A、电解饱和食盐水制烧碱,在阳极区产生NaOH溶液 |
| B、电解法精炼粗铜,用纯铜作阴极 |
| C、电解熔融的氯化钠制取金属钠,金属钠在阴极产生 |
| D、在镀件上电镀银,用银作阳极 |
下列物质转化在给定条件下能实现的是( )
①Al2O3
NaAlO2(aq)
Al(OH)3
②S
SO3
H2SO4
③饱和NaCl(aq)
NaHCO3
Na2CO3
④Fe2O3
FeCl2
无水FeCl3
⑤MaCl2(aq)
Mg(OH)2
煅烧MgO.
①Al2O3
| NaOH(aq) |
| △ |
| CO2 |
②S
| O2点燃 |
| H2O |
③饱和NaCl(aq)
| NH3CO2 |
| △ |
④Fe2O3
| HCl(aq) |
| △ |
⑤MaCl2(aq)
| 石灰乳 |
| 燃烧 |
| A、①③⑤ | B、②③④ |
| C、②④⑤ | D、①④⑤ |
简单原子的原子结构可用下图形象的表示:① ②
②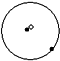 ③
③
其中 表示质子或电子,
表示质子或电子, 表示中子,则下列有关的叙述正确的是( )
表示中子,则下列有关的叙述正确的是( )
 ②
② ③
③
其中
 表示质子或电子,
表示质子或电子, 表示中子,则下列有关的叙述正确的是( )
表示中子,则下列有关的叙述正确的是( )| A、①②③为同素异形体 |
| B、①②③互为同位素 |
| C、①②③是三种化学性质不同的粒子 |
| D、①②③具有相同的质量数 |
