题目内容
下列分子的立体结构,其中属于直线型分子的是( )
| A、H2O |
| B、CO2 |
| C、C2H4 |
| D、P4 |
考点:判断简单分子或离子的构型
专题:化学键与晶体结构
分析:价层电子对互斥模型(简称VSEPR模型),根据价电子对互斥理论,价层电子对个数=σ键个数+孤电子对个数.σ键个数=配原子个数,孤电子对个数=
×(a-xb),a指中心原子价电子个数,x指配原子个数,b指配原子形成稳定结构需要的电子个数;分子的立体构型是指分子中的原子在空间的排布,不包括中心原子未成键的孤对电子;实际空间构型要去掉孤电子对,略去孤电子对就是该分子的空间构型.
价层电子对个数为4,不含孤电子对,为正四面体结构;含有一个孤电子对,空间构型为三角锥形,含有两个孤电子对,空间构型是V型;
价层电子对个数为3,不含孤电子对,平面形结构;含有一个孤电子对,空间构型为为V形结构;
价层电子对个数是2且不含孤电子对,为直线形结构,据此判断.
| 1 |
| 2 |
价层电子对个数为4,不含孤电子对,为正四面体结构;含有一个孤电子对,空间构型为三角锥形,含有两个孤电子对,空间构型是V型;
价层电子对个数为3,不含孤电子对,平面形结构;含有一个孤电子对,空间构型为为V形结构;
价层电子对个数是2且不含孤电子对,为直线形结构,据此判断.
解答:
解:A.水分子中价层电子对个数=2+
×(6-2×1)=4,含有2个孤电子对,略去孤电子对后,实际上其空间构型是V型,故A错误;
B.二氧化碳分子中价层电子对个数=σ键个数+孤电子对个数=2+
(4-2×2)=2,不含孤电子对,所以空间构型是直线形,故B正确;
C.C2H4分子中价层电子对=σ 键电子对+中心原子上的孤电子对=3+0=3,分子中不含孤电子对,所以其空间构型是平面形结构,故C错误;
D.白磷P4的结构式为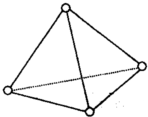 ,P原子最外层电子数是5,每个P原子形成3个共价键,P4属于正四面体结构,故D错误;
,P原子最外层电子数是5,每个P原子形成3个共价键,P4属于正四面体结构,故D错误;
故选B.
| 1 |
| 2 |
B.二氧化碳分子中价层电子对个数=σ键个数+孤电子对个数=2+
| 1 |
| 2 |
C.C2H4分子中价层电子对=σ 键电子对+中心原子上的孤电子对=3+0=3,分子中不含孤电子对,所以其空间构型是平面形结构,故C错误;
D.白磷P4的结构式为
 ,P原子最外层电子数是5,每个P原子形成3个共价键,P4属于正四面体结构,故D错误;
,P原子最外层电子数是5,每个P原子形成3个共价键,P4属于正四面体结构,故D错误;故选B.
点评:本题考查了分子的立体构型的判断,侧重分子结构与性质的考查,注意杂化轨道理论的理解应用,把握常见分子中原子的杂化及空间构型为解答的关键,题目难度中等.

练习册系列答案
相关题目
如表为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是( )


| A、常压下五种元素的单质中,Z单质的沸点最高 |
| B、Y、Z的阴离子电子层结构都与R原子的相同 |
| C、Y的氢化物的沸点比H2O的沸点高 |
| D、Y元素的非金属性比W元素的非金属性强 |
元素周期表中,在金属元素和非金属元素的分界线附近能找到的元素是( )
| A、研制新型农药的元素 |
| B、制造半导体材料的元素 |
| C、制造催化剂的元素 |
| D、制造耐高温合金的元素 |
下列涉及有机化合物的说法正确的是( )
| A、苯中含有三个碳碳双键,所以苯可以与氢气发生加成反应 |
| B、乙炔可以用作植物生长调节剂 |
| C、甲醛是制造酚醛树脂的原料 |
| D、苯和乙烯都能使溴水褪色,其褪色原理是相同的 |
下列说法正确的是( )
A、还原性染料靛蓝的结构简式为: ,它的分子式是:C16H10N2O2 ,它的分子式是:C16H10N2O2 |
| B、结构为…-CH=CH-CH=CH-CH=CH-CH=CH-…的高分子化合物,其单体是乙烯 |
| C、总质量一定时,乙炔和乙醛无论按什么比例混合,完全燃烧消耗氧气量或生成CO2量不变 |
| D、丙烯酸(CH2=CHCOOH)和山梨酸(CH3CH=CHCH=CHCOOH)不是同系物,它们与氢气 充分反应后的产物也不是同系物 |
 如图的实验装置用来分离CO2和CO气体并干燥.图中a为止水夹,b为分液漏斗的活塞,通过Y形管和止水夹分别接c、d两球胆,现装置内的空气已排尽.为使实验成功,甲、乙、丙中盛放的溶液分别为( )
如图的实验装置用来分离CO2和CO气体并干燥.图中a为止水夹,b为分液漏斗的活塞,通过Y形管和止水夹分别接c、d两球胆,现装置内的空气已排尽.为使实验成功,甲、乙、丙中盛放的溶液分别为( )| A、NaHCO3饱和溶液、12 mol?L-1 盐酸,18.4 mol?L-1 H2SO4 |
| B、Na2CO3饱和溶液、2 mol?L-1 H2SO4、NaOH饱和溶液 |
| C、NaOH饱和溶液、2 mol?L-1 H2SO4、18.4 mol?L-1 H2SO4 |
| D、18.4 mol?L-1 H2SO4、NaOH饱和溶液、18.4 mol?L-1 H2SO4 |
下列物质的水溶液中,是由于促进了水的电离而呈酸性的是( )
| A、H2SO4 |
| B、NH4Cl |
| C、NaCl |
| D、CH3COONa |
把下列四种碳酸氢钠溶液分别加入四个盛有10mL 2mol?L-1盐酸的烧杯中,均加水稀释到50mL,此时碳酸氢钠和盐酸反应,其中反应开始时速率最大的是( )
| A、10℃20 mL 3 mol?L-1的碳酸氢钠溶液 |
| B、20℃30 mL 2 mol?L-1的碳酸氢钠溶液 |
| C、20℃10 mL 4 mol?L-1的碳酸氢钠溶液 |
| D、10℃20 mL 2 mol?L-1的碳酸氢钠溶液 |
下列反应中,既属于氧化还原反应同时又是吸热反应的是( )
| A、Ba(OH)2.8H2O与NH4Cl反应 |
| B、铝与稀盐酸 |
| C、灼热的炭与CO2反应 |
| D、甲烷与O2的燃烧反应 |