题目内容
14.下列各组元素中,按最高正化合价递减的顺序排列的是( )| A. | C、N、O | B. | S、P、Si | C. | F、O、Br | D. | H、Ca、Al |
分析 同周期从左向右最高正价增大,O、F无正价,结合元素在周期表中的位置判断,以此来解答.
解答 解:A.C、N、O的最高正价分别为+4、+5、0,故A不选;
B.S、P、Si的最高正价分别为+6、+5、+4,最高正化合价递减,故B选;
C.F、O、Br的最高正价分别为0、0、+7,故C不选;
D.H、Ca、Al的最高正价分别为+1、+2、+3,最高正化合价递增,故D不选;
故选B.
点评 本题考查元素周期表及元素周期律,为高频考点,把握元素最高正价与最外层电子数的关系为解答的关键,侧重分析与应用能力的考查,注意O、F无正价,题目难度不大.

练习册系列答案
相关题目
18.设NA为阿伏加德罗常数的值.下列叙述正确的是( )
| A. | 1molFe溶于硝酸,电子转移数为3NA | |
| B. | 12.0gNaHSO4固体中含阳离子数为0.1NA | |
| C. | 标准状态下,22.4L氟化氢中含有氟原子数为NA | |
| D. | 7.8gNa2O2与足量的水反应转移电子数为0.2NA |
5.现有四种短周期元素的原子半径及主要化合价数据如表所示:
下列叙述不正确的是( )
| 元素 | 甲 | 乙 | 丙 | 丁 |
| 原子半径/nm | 0.186 | 0.102 | 0.152 | 0.074 |
| 主要化合价 | +1 | +6、-2 | +1 | -2 |
| A. | 甲的最高价氧化物对应水化物的碱性比丙的强 | |
| B. | 甲单质可用电解其盐溶液的方法冶炼而得 | |
| C. | 常温下,丁的两种氢化物均为液体 | |
| D. | 乙的简单离子是四种元素各自形成的简单离子中半径最大的 |
9.下列各种醇不能被氧化成醛或酮的是(提示:酮的结构为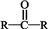 )( )
)( )
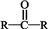 )( )
)( )| A. | CH3OH | B. | 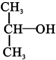 | C. | 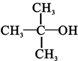 | D. | 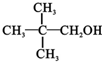 |
19.下列说法中,错误的是( )
| A. | 无论是乙烯分子还是苯分子,它们分子中所有原子都是在同一个平面上 | |
| B. | 无论使用溴的四氯化碳溶液还是酸性KMnO4溶液都可以鉴别乙烯和乙烷 | |
| C. | 无论是足量的乙醇还是乙酸,它们与等质量的钠反应,相同条件下产生的气体体积相同 | |
| D. | 无论是植物油还是动物脂肪它们都属于饱和高级脂肪酸甘油酯 |
3.用R元素代表短周期元素,R原子最外层p能级上有2个未成对电子.下列关于R的描述正确的是( )
| A. | R的氧化物都能溶于水 | |
| B. | R的最高价氧化物对应的水化物都是H2RO4 | |
| C. | R一定是非金属元素 | |
| D. | R的最高价氧化物都能与NaOH溶液反应 |
4.常温下,将铜片投入到下列溶液中,会产生气体的是( )
| A. | 稀硫酸 | B. | 浓盐酸 | C. | 稀硝酸 | D. | 浓硫酸 |
 ④癸烷⑤CH3COOH ⑥
④癸烷⑤CH3COOH ⑥ ⑦
⑦ ⑧
⑧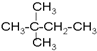 ⑨丙烷
⑨丙烷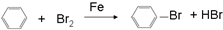 ;
; ;
;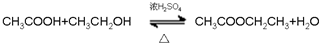 .
.