题目内容
10.既有离子键又有共价键和配位键的化合物是( )| A. | HN03 | B. | Ba(OH)2 | C. | (NH4)2SO4 | D. | H2O |
分析 一般来说,活泼金属和活泼非金属元素之间易形成离子键,非金属元素之间易形成共价键,含有孤电子对的原子和含有空轨道的原子之间存在配位键,据此分析解答.
解答 解:A.元素之间以共价键相结合,所以只存在共价键,故A错误;
B.氢氧化钡中钡离子和氢氧根离子之间存在离子键,氧原子和氢原子之间存在共价键,不含配位键,故B错误;
C.硫酸铵中铵根离子和硫酸根离子之间存在离子键,氮原子和氢原子、氮原子和氧原子之间存在共价键,铵根离子还存在配位键,故C正确;
D.水分子中氢原子和氧原子之间存在共价键,不含离子键和配位键,故D错误.
故选:C.
点评 本题考查了化学键的判断,根据离子键和共价键的概念来分析解答即可,注意配位键也属于共价键,但氢键不属于共价键,属于分子间作用力,为易错点.

练习册系列答案
相关题目
4.一种新型钠硫电池结构示意图如图,下列有关该电池的说法正确的是( )


| A. | B极中填充多孔的炭或石墨毡,目的是为了增加导电性 | |
| B. | 电池放电时,A极电极反应为:2Na++xS+2 e-=Na2SX | |
| C. | 电池放电时,Na+向电极A极移动 | |
| D. | 电池放电的总反应为2Na+xS=Na2SX,每消耗1molNa转移2mol电子 |
5.有a、b、c、d四种元素,原子序数依次增大.a存在a+和a-两种离子,b和c为同一主族元素,c的次外层有8个电子,c2-和d2+的电子层结构相同.下列叙述正确的是( )
| A. | b、c与a形成化合物的稳定性一定为b>c | |
| B. | a和d形成的化合物与水反应产生气体可以作燃料 | |
| C. | c,a和b可形成的化合物为离子化合物 | |
| D. | a、b、c、d四种元素组成的化合物的水溶液可以为酸性、也可以为碱性 |
2.下列体系加压后,对化学反应速率没有影响的是( )
| A. | 2SO2+O2?2SO3 | B. | CO+H20(气)?CO2+H2 | ||
| C. | CO2+H2O?H2CO3 | D. | NaOH+HCl=NaCl+H20 |
5.为了除去粗盐中的Ca2+、Mg2+、SO42-及泥沙,可将粗盐溶于水,然后进行以下五项操作:①过滤;②加过量NaOH溶液;③加适量稀盐酸;④加过量Na2CO3溶液;⑤加过量BaCl2溶液,正确的是( )
| A. | ⑤②④①③ | B. | ④①②⑤③ | C. | ①④②⑤③ | D. | ②④⑤①③ |
15.下列化学用语表达正确的是( )
| A. | 溴化铵的电子式: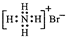 | B. | CO2的电子式: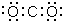 | ||
| C. | HClO的结构式:H-Cl-O | D. | 氮分子的结构式:N≡N |
2.碱金属和卤素随着原子序数的增大,下列递变规律正确的是( )
| A. | 碱金属单质的熔、沸点逐渐降低 | B. | 卤素单质的熔、沸点逐渐降低 | ||
| C. | 碱金属单质的密度逐渐增大 | D. | 卤素单质的密度逐渐减小 |
19.现有A~I 9种短周期元素,它们在元素周期表中的位置如下.请据此回答下列问题:
(1)下列中的元素的原子间反应最容易形成离子键的是B
A.C和F B.B和G C.D和G D.B和E
(2)下列由A~G形成的各分子中所有原子都满足最外层为8电子结构的是D.
A.EA3 B.AG C.FG5 D.DG4
(3)由A、E组成的一种化合物化学式为EA5,其各原子均达到同周期稀有气体原子的稳定结构,试写出该化合物的电子式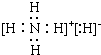 .
.
(4)B,C,H,G形成的简单离子半径由大到小S2->Cl->Na+>Al3+
(5)A与I形成1:1的化合物的结构式为H-O-O-H
(6)写出B的最高价氧化物的水化物与G的最高价氧化物的水化物反应方程式:NaOH+Al(OH)3=NaAlO2+2H2O
写出HI2使酸性高锰酸钾褪色的离子方程式:5SO2+2MnO4-+2H2O=5SO42-+2Mn2++4H+.
| A | |||||||||||||||||
| D | E | I | |||||||||||||||
| B | C | F | H | G | |||||||||||||
A.C和F B.B和G C.D和G D.B和E
(2)下列由A~G形成的各分子中所有原子都满足最外层为8电子结构的是D.
A.EA3 B.AG C.FG5 D.DG4
(3)由A、E组成的一种化合物化学式为EA5,其各原子均达到同周期稀有气体原子的稳定结构,试写出该化合物的电子式
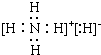 .
.(4)B,C,H,G形成的简单离子半径由大到小S2->Cl->Na+>Al3+
(5)A与I形成1:1的化合物的结构式为H-O-O-H
(6)写出B的最高价氧化物的水化物与G的最高价氧化物的水化物反应方程式:NaOH+Al(OH)3=NaAlO2+2H2O
写出HI2使酸性高锰酸钾褪色的离子方程式:5SO2+2MnO4-+2H2O=5SO42-+2Mn2++4H+.
20.化学在生产和日常生活中有着重要的应用.下列叙述正确的是( )
| A. | 钢铁设备与直流电源正极相连可防腐 | |
| B. | 明矾水解时产生具有吸附性的胶体粒子,可以用于饮用水的杀菌消毒 | |
| C. | 开启啤酒瓶后,瓶中立刻泛起大量泡沫不能用勒夏特列原理解释 | |
| D. | 废旧电池中的汞、锅、铅等重金属盐对土壤和水源会造成污染 |