题目内容
7.下列关于原子核外电子排布与元素在周期表中位置关系的表述中,正确的是( )| A. | 原子的价电子排布为ns2np1~6的元素一定是主族元素 | |
| B. | 基态原子的p能级上有5个电子的元素一定是ⅦA族元素 | |
| C. | 原子的价电子排布为(n-1)d6~8ns2的元素一定位于ⅢB~ⅦB族 | |
| D. | 基态原子的N层上只有1个电子的元素一定是主族元素 |
分析 A、零族元素价电子排布也符合ns2np1~6;
B、基态原子的p能级上有5个电子的元素价电子排布为ns2np5的元素;
C、原子的价电子排布为(n-1)d6-8ns2的元素为Ⅷ族元素;
D、基态原子的N层上只有一个电子的元素,可能为K、Cr或Cu.
解答 解:A、零族元素价电子排布也符合ns2np1~6,所以不一定是主族元素,故A错误;
B、基态原子的p能级上有5个电子的元素价电子排布为ns2np5的元素,一定位于ⅦA族,故B正确;
C、原子的价电子排布为(n-1)d6-8ns2的元素为Ⅷ族元素,不是位于ⅢB~ⅦB族,故C错误;
D、基态原子的N层上只有一个电子的元素,可能为K、Cr或Cu,K为主族元素,Cr、Cu为副族元素,故D错误;
故选B.
点评 本题考查结构与位置关系、元素周期表,难度不大,侧重对过渡元素的考查,注意把握元素周期表的结构,Ⅷ族元素的结构特点.

练习册系列答案
相关题目
3.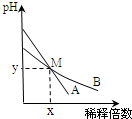 室温下,pH相差1的两种一元碱溶液A和B,分别加水稀释时,溶液的pH变化如图所示.下列说法正确的是( )
室温下,pH相差1的两种一元碱溶液A和B,分别加水稀释时,溶液的pH变化如图所示.下列说法正确的是( )
 室温下,pH相差1的两种一元碱溶液A和B,分别加水稀释时,溶液的pH变化如图所示.下列说法正确的是( )
室温下,pH相差1的两种一元碱溶液A和B,分别加水稀释时,溶液的pH变化如图所示.下列说法正确的是( )| A. | 稀释前,c(A)=10c(B) | |
| B. | 稀释前,A溶液中由水电离出的OH-的浓度大于10-7mol/L | |
| C. | 用醋酸中和A溶液至恰好完全反应时,溶液的pH为7 | |
| D. | 在M点,A、B两种碱溶液中阳离子的物质的量浓度相等 |
4.下列物质中,可一次性鉴别乙酸、乙醇、苯的是( )
| A. | 氢氧化钠溶液 | B. | 溴水 | C. | 碳酸钠溶液 | D. | 稀硫酸 |
1.一定条件下,某容器中各微粒在反应前后变化的示意图如下,其中 和
和 代表不同元素的原子.
代表不同元素的原子.
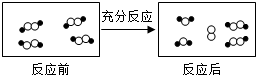
关于此反应说法错误的是( )
 和
和 代表不同元素的原子.
代表不同元素的原子.
关于此反应说法错误的是( )
| A. | 一定属于吸热反应 | B. | 一定属于可逆反应 | ||
| C. | 一定属于氧化还原反应 | D. | 一定属于分解反应 |
2.现有四种元素的基态原子的外围电子排布式如下:①ns2np3 ②ns2np4 ③ns2np5④ns2np6则下列有关比较中正确的是( )
| A. | 原子半径最大的主族元素是④ | B. | 电负性最大的元素是① | ||
| C. | 第一电离能最小的元素是② | D. | ③的最高正化合价一定是+7价 |
12.下列物质中,不具有漂白作用的是( )
| A. | 活性炭 | B. | 氯气 | C. | 次氯酸溶液 | D. | 二氧化碳 |
19.以下互为同位素的是( )
| A. | 14C与14N | B. | D2与H2 | C. | O2与O3 | D. | 35Cl与37Cl |
16.下列说法中,正确的是( )
| A. | 铝是一种既可以与强酸反应又可以与强碱反应的金属 | |
| B. | 氧化铝按组成划分属于金属氧化物,按性质划分属于碱性氧化物 | |
| C. | 氢氧化铝具有较高的熔点和沸点,常用于制造耐火材料 | |
| D. | 铝是地壳中含量最多的元素,铝土矿是铝元素在地壳中的主要存在形式之一 |
17.与27.0克H2O含有相同中子数的D2O质量为( )
| A. | 13.2g | B. | 20.1g | C. | 24.0g | D. | 30.0g |