��Ŀ����
11�����мס��ҡ������������������ӻ������γɵ���Һ���ֱ���K+��NH4+��Ag+��Ba2+��Fe3+��Cl-��OH-��CO32-��SO42-��NO3-�е������Ӻ������Ӹ�һ����ɣ��������ӻ������������������Ӹ�����ͬ������֪��������ʱ��0.1mol•L-1����Һ��pH=10���ڱ���������������Һ��pH��С��7���۱���Һ�ֱ�������������Һ��Ӧ�����ɳ������ܼ���Һ�붡��Һ�ڼ��������·�Ӧ�Ȳ�����ɫ�����ֲ����̼�����ζ�����壬���ɵİ�ɫ����������ϡ���ᣮ��������ʵ����ʵ�����ƶϣ�������| A�� | ��ΪK2SO4��Һ | B�� | ��ΪK2CO3��Һ | C�� | ��ΪFe��NO3��3��Һ | D�� | ��Ϊ��NH4��2SO4��Һ |
���� ���ݸ����������ʺ�������жϣ�K+��NH4+��Ag+��Ba2+��Fe3+��Cl-��OH-��CO32-��SO42-��NO3-��Ag+��ֻ�ܺ���������ӹ����γɵ�����ΪAgNO3��
������ʱ��0.1mol•L-1����Һ��pH=10��֤����������Һˮ���Լ��Ե����ʣ��ж���ΪK2CO3��
�ڱ���������������Һ��pH��С��7����Һ��ˮ�������Ե����ʣ�����������ˮ���ж�ΪAgNO3��FeCl3����NH4��2SO4����Fe2��SO4��3��NH4Cl��
�۱���Һ�ֱ�������������Һ��Ӧ�����ɳ�����������������жϱ�ΪAgNO3��
�ܼ���Һ�붡��Һ�ڼ��������·�Ӧ�Ȳ�����ɫ�����ֲ����̼�����ζ�����壬���ɵİ�ɫ����������ϡ���ᣬ˵����ΪBa��OH��2����Ϊ��NH4��2SO4������ΪFeCl3���Դ˽����⣮
��� �⣺�ס��ҡ������������������ӻ������γɵ���Һ���������ӻ������������������Ӹ�����ͬ�����ݸ����������ʺ�������жϣ�K+��NH4+��Ag+��Ba2+��Fe3+��Cl-��OH-��CO32-��SO42-��NO3-��Ag+��ֻ�ܺ���������ӹ����γɵ�����ΪAgNO3��
������ʱ��0.1mol•L-1����Һ��pH=10��֤����������Һˮ���Լ��Ե����ʣ��������ж�Ϊ̼������ӣ�������Ϊ�����ӣ��ж���ΪK2CO3��
�ڱ���������������Һ��pH��С��7����Һ��ˮ�������Ե����ʣ�����������ˮ���ж�ΪAgNO3��FeCl3����NH4��2SO4����Fe2��SO4��3��NH4Cl��
�۱���Һ�ֱ�������������Һ��Ӧ�����ɳ�������������������жϣ���ΪAgNO3��
�ܼ���Һ�붡��Һ�ڼ��������·�Ӧ�Ȳ�����ɫ�����ֲ����̼�����ζ�����壬���ɵİ�ɫ����������ϡ���ᣬ˵����ΪBa��OH��2����Ϊ��NH4��2SO4������ΪFeCl3��
������������ΪBa��OH��2����ΪK2CO3����ΪAgNO3����Ϊ��NH4��2SO4����ΪFeCl3��
��ѡBD��
���� ���⿼��������ƶϣ�Ϊ��Ƶ���㣬������ѧ���ķ���������ʵ�������Ŀ��飬��Ŀ�е���Ϣ�ǽ���ؼ�������Һ��ʹ��ɫʯ����Һ��졢��Һ�ʼ��ԡ����ɰ�ɫ����������ȣ�ͬʱǰ����ϵ�����ھ������������Ϣ�����ܼ������������⣬��Ŀ�Ѷ��еȣ�

| A�� | �٢ڢ� | B�� | �٢ڢ� | C�� | �ڢݢ� | D�� | �٢ڢ� |
| A�� | ú����õ���ú���ͣ�����Ҫ��;�����پ�����õ���Ʒ��ȼ�ͣ���һ�����������֡���̼��������� | |
| B�� | ��¯ˮ���к��е�CaSO4��������Na2CO3��Һ�������������ȥ | |
| C�� | ���챦ʯ������ʯ����Ҫ�ɷ���������������ɡ�ʯӢ����������ɸ����Ҫ�ɷ��ǹ����� | |
| D�� | ���������������ڽ��ػ����������������ָ��£������������ǽ������� |
| A�� | ���������������������� | B�� | �����û��������е��� | ||
| C�� | ��������������ɫ�Ľ��� | D�� | ��������+3�۵Ļ����� |
| A�� | NaOH��Һ������������� | B�� | ��������������� | ||
| C�� | ����Ӧ��ת�Ƶĵ�������� | D�� | ��Ӧ������Һ��pH��С��7 |
��1��CO2��H2��һ�������¿���������ϩ��6H2��g��+2CO2��g��+CH2�TCH2��g��+4H2O��g����H=a kJ•mol-1
��֪��H2��g����ȼ����Ϊ285.8kJ•mol-1��CH2=CH2��g����ȼ����Ϊ1411.0kJ•mol-1��H2O��g��=H2O��l����H=-44.0kJ•mol-1����a=-127.8kJ•mol-1��
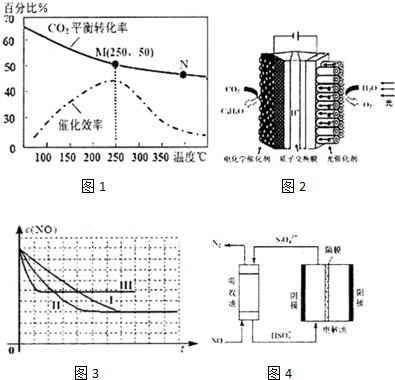
��2������������ϩ�ķ�Ӧ�У��¶ȶ�CO2��ƽ��ת���ʼ������Ĵ�Ч��Ӱ����ͼ1�������й�˵������ȷ���Ǣ٢ڢܣ�����ţ�
���¶�Խ�ߣ������Ĵ�Ч��Խ��
���·�����250��ʱ�������¶����ߣ���ϩ�IJ�������
��M��ƽ�ⳣ����N��ƽ�ⳣ����
��N������Ӧ����һ������M������Ӧ����
������ѹǿ�������ϩ���������
��3��2012���ѧ�Ҹ��ݹ������ԭ�����Ƴ���������Ҷ������ͼ2�ǡ�������Ҷ���ĵ绯ѧģ��ʵ��װ��ͼ����װ���ܽ�H2O��CO2ת��ΪO2���л���C3H8O�������ĵ缫��ӦʽΪ��3CO2+18H++18e-=C3H8O+5H2O
II��Ϊ���������Ⱦ����������β���ŷŴ���װ��ת��װ�ã���Ӧ����ʽΪ��2NO��g��+2CO��g��?2CO2��g��+N2��g����
��4��������Ӧʹ�õ�������ij�ִ���ʱ���¶Ⱥʹ����ıȱ�����Ի�ѧ��Ӧ���ʵ�Ӱ��Ա�ʵ�����±���c��NO��Ũ����ʱ�䣨t���仯������3ͼ��
| ��� | T���棩 | NO��ʼŨ�ȣ�mol/L�� | CO��ʼŨ�ȣ�mol/L�� | �����ıȱ������m2/g�� |
| �� | 280 | 1.20��10-3 | 5.80��10-3 | 82 |
| �� | 280 | a | 5.80��10-3 | 124 |
| �� | 350 | 1.20��10-3 | 5.80��10-3 | b |
��ʵ��˵�����÷�Ӧ�Ƿ��ȷ�Ӧ������ȡ������ȡ�����
������500��ʱ��Ͷ��$\frac{c��NO��}{c��CO��}$=1��NO��ת����Ϊ80%������¶�ʱ��ƽ�ⳣ��K=��һ���������c��NO��=1mol•L-1����K=160��
�ڶ����������c��NO��=amol•L-1����K=$\frac{160}{a}$��
�������������n��NO��=amol���������ݻ�ΪV L����K=$\frac{160V}{a}$����
��5��ʹ�õ绯ѧ��Ҳ�ɴ���NO����Ⱦ��װ����ͼ4����֪��������������Һ��pH��4��7֮�䣬д�������ĵ缫��Ӧʽ��2HSO3-+2H++2e-=S2O42-+2H2O�����ճ��г�ȥNO�����ӷ���ʽΪ��2NO+2S2O42-+2H2O=N2+4HSO3-��
| A�� | X����̬�⻯���Y����̬�⻯���ȶ� | |
| B�� | Xԭ�ӵĵ��Ӳ�����Yԭ�ӵĵ��Ӳ����� | |
| C�� | Y�ĵ����ܽ�X��NaX����Һ���û����� | |
| D�� | Y�ڰ�������H2��Ӧ��X�ڼ��������²�����H2��Ӧ |