题目内容
16.过氧化氢俗名双氧水,医疗上利用它杀菌消毒.根据下列反应回答问题:(1)下述四个反应中,H2O2仅体现氧化性的反应是D(填序号,下同);
H2O2既体现氧化性又体现还原性的反应是C.
A.Na2O2+2HCl=2NaCl+H2O2
B.Ag2O+H2O2=2Ag+O2↑+H2O
C.2H2O2=2H2O+O2↑
D.3H2O2+Cr2(SO4)3+10KOH=2K2CrO4+3K2SO4+8H2O
(2)上述反应说明H2O2、Ag2O、K2CrO4的氧化性由强到弱的顺序是Ag2O>H2O2>K2CrO4.
(3)某酸性反应体系中发生的一个氧化还原的离子反应,反应物和生成物共六种微粒:O2、MnO4-、H2O、Mn2+、H2O2、H+己知该反应中H2O2只发生了如下过程:H2O2→O2.
①写出上述反应的离子方程式并配平:2MnO4-+5H2O2+6H+=2Mn2++8H2O+5O2↑.
②如果上述反应中有6.72L(标准状况)气体生成,转移的电子为0.6mol.
分析 (1)双氧水体现氧化性说明双氧水中元素化合价仅降低,既体现氧化性又体现还原性说明双氧水中元素化合价既升高又降低;
(2)氧化剂的氧化性>氧化产物的氧化性>还原剂的氧化性;
(3)①根据氧化还原反应中氧化剂和还原剂的特点和性质来寻找反应物和生成物,然后结合化合价升降相等配平;
②根据所发生的反应来分析化合价的变化情况,进而得到转移电子的数目.
解答 解:(1)D中双氧水中氧元素化合价仅降低,说明仅体现氧化性,C中双氧水中氧元素化合价化合价既升高又降低,则既体现氧化性又体现还原性,故答案为:D;C;
(2)反应Ag2O+H2O2=2Ag+O2↑+H2O中,氧化银做氧化剂,双氧水作还原剂,则氧化性Ag2O>H2O2,反应3H2O2+Cr2(SO4)3+10KOH=2K2CrO4+3K2SO4+8H2O中,双氧水做氧化剂,铬酸钾做氧化产物,则氧化性H2O2>K2CrO4,故氧化性顺序为:Ag2O>H2O2>K2CrO4,
故答案为:Ag2O>H2O2>K2CrO4;
(3)①该反应过程中,高锰酸根的氧化性和双氧水的还原性导致二者间发生氧化还原反应,高锰酸根离子中锰元素从+7变为+2价,化合价降低5价,双氧水中氧元素化合价从-1价变为0价,化合价至少升高2价,则高锰酸根离子的系数为2,双氧水的系数为5,然后利用质量守恒配平可得该反应的离子方程式为:2MnO4-+5H2O2+6H+=2Mn2++8H2O+5O2↑,
故答案为:2MnO4-+5H2O2+6H+=2Mn2++8H2O+5O2↑;
②上述反应中生成5mol氧气转移电子10mol,当反应中有6.72L(标准状况)即0.3mol氧气生成时,则转移的电子为:10mol×$\frac{0.3mol}{5}$=0.6mol,
故答案为:0.6.
点评 本题考查了氧化还原反应的配平及综合应用,题目难度中等,试题知识点较多、综合性较强,充分考查学生的分析、理解能力及灵活应用能力,注意掌握氧化还原反应的配平方法,明确氧化剂、还原剂的概念及判断方法.

 名校作业本系列答案
名校作业本系列答案 轻巧夺冠周测月考直通名校系列答案
轻巧夺冠周测月考直通名校系列答案 甲醇是一种可再生能源,具有广泛的开发和应用前景.
甲醇是一种可再生能源,具有广泛的开发和应用前景.(1)工业上一般采用下列两种反应合成甲醇:
反应Ⅰ:CO(g)+2H2(g)?CH3OH(g)△H 1
反应Ⅱ:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H 2
①表所列数据是反应Ⅰ在不同温度下的化学平衡常数(K).
| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
②某温度下,将2molCO和6molH2充入2L的密闭容器中,充分反应,达到平衡后,测得c(CO)=0.2mol/L,则CO的转化率为80%,此时的温度为250℃(从上表中选择).
(2)已知在常温常压下:
①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g)△H1=-1275.6kJ/mol
②2CO (g)+O2(g)=2CO2(g)△H2=-566.0kJ/mol
③H2O(g)=H2O(l)△H3=-44.0kJ/mol
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:CH3OH(l)+O2(g)=CO(g)+2 H2O(l)△H=-442.8kJ•mol-1
(3)某实验小组依据甲醇燃烧的反应原理,设计如图所示的电池装置:
①该电池正极的电极反应为O2+2H2O+4e-=4OH-
②该电池总反应的离子方程式为2CH3OH+3O2+4OH-=2CO32-+6H2O
③工作一段时间后,测得溶液的pH减小(填“增大”、“减小”或“不变”).
| A. | c(B2-)+c(HB-)=0.1 mol/L | B. | c(B2-)+c(HB-)+c(H2B)=0.1 mol/L | ||
| C. | c(OH-)=c(H+)+c(HB-)+2c(H2B) | D. | c(Na+)+c(OH-)=c(H+)+c(HB-) |
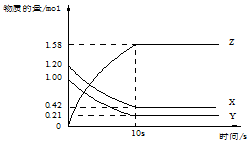 一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示:下列描述正确的是( )
一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示:下列描述正确的是( )| A. | 反应开始到10s,用Z表示的反应速率为0.158mol/(L•s) | |
| B. | 反应开始到10s,X的物质的量浓度减少了0.79mol/L | |
| C. | 反应的化学方程式为:X(g)+Y(g)?Z(g) | |
| D. | 反应开始到10s时,Y的转化率为79.0% |
①BF3 ②CH3═CH2 ③苯 ④CH≡CH ⑤NH3 ⑥CH4 ⑦HCHO.
| A. | ①②③⑦ | B. | ①⑤⑥ | C. | ②③④⑦ | D. | ③⑤⑥ |
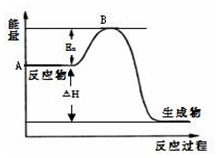 2SO2(g)+O2(g)?2SO3(g)△H=a kJ•mol-1,反应过程的能量变化如图所示.已知1mol SO2(g)完全转化为1mol SO3(g)放热99kJ.请回答:
2SO2(g)+O2(g)?2SO3(g)△H=a kJ•mol-1,反应过程的能量变化如图所示.已知1mol SO2(g)完全转化为1mol SO3(g)放热99kJ.请回答: