题目内容
15.在标准状况下,气体A的密度是3.170g/L,则A的摩尔质量为71g/mol.分析 标况下,气体摩尔体积为22.4L/mol,根据ρ=$\frac{M}{{V}_{m}}$计算A的摩尔质量.
解答 解:标况下,气体摩尔体积为22.4L/mol,根据ρ=$\frac{M}{{V}_{m}}$知A的摩尔质量=ρVm=3.170g/L×22.4L/mol=71g/mol,
故答案为:71g/mol.
点评 本题考查物质的量的计算,为高频考点,侧重考查学生分析计算能力,明确密度与摩尔质量关系是解本题关键,题目难度不大.

练习册系列答案
 轻松暑假总复习系列答案
轻松暑假总复习系列答案
相关题目
6.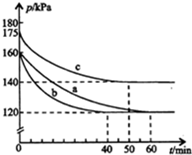 在容积为2L的密闭容器中进行反应:AX3(g)+X2(g)?AX5(g)△H=QkJ/mol,起始时AX3和X2均为1.0mol.反应在不同条件下进行,反应体系总压强随时间的变化如图所示.下列有关说法不正确的是( )
在容积为2L的密闭容器中进行反应:AX3(g)+X2(g)?AX5(g)△H=QkJ/mol,起始时AX3和X2均为1.0mol.反应在不同条件下进行,反应体系总压强随时间的变化如图所示.下列有关说法不正确的是( )
 在容积为2L的密闭容器中进行反应:AX3(g)+X2(g)?AX5(g)△H=QkJ/mol,起始时AX3和X2均为1.0mol.反应在不同条件下进行,反应体系总压强随时间的变化如图所示.下列有关说法不正确的是( )
在容积为2L的密闭容器中进行反应:AX3(g)+X2(g)?AX5(g)△H=QkJ/mol,起始时AX3和X2均为1.0mol.反应在不同条件下进行,反应体系总压强随时间的变化如图所示.下列有关说法不正确的是( )| A. | Q<0 | |
| B. | 与实验a相比,实验b加入了催化剂 | |
| C. | 实验b条件下,该反应的平衡常数K=2 | |
| D. | 实验c从反应开始至达到平衡时的平均反应速率为v(AX5)=4.0×10-3mol/(L•min) |
10.如图是实验室制备氯气并验证氯气性质的装置(其中夹持装置已省略)
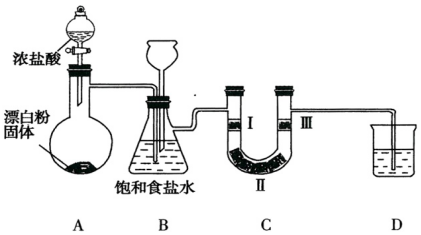
已知:装置A是氯气的发生装置,反应的化学方程式为:
Ca(ClO)2+4HCl(浓)═CaCl2+2Cl2↑+2H2O.
据此回答下列问题:
(1)装置B中饱和食盐水的作用是除去Cl2中的HCl.
(2)装置B也是安全瓶,目的是监测实验进行时装置C中是否发生堵塞,请写出装置C中发生堵塞时装置B中的实验现象:B中长颈漏斗中液面上升.
(3)装置C的目的是验证氯气是否具有漂白性,则装置C中Ⅰ、Ⅱ、Ⅲ处依次应放入的物质是d(填序号).
(4)装置D的作用是吸收多余的氯气,防止污染空气,则烧杯中的溶液是NaOH溶液,写出所发生反应的化学方程式:Cl2+2NaOH=NaCl+NaClO+H2O.
(5)若所用浓盐酸的浓度为10mol/L,求产生2.24L(标准状况)Cl2时,发生反应的盐酸为40mL.

已知:装置A是氯气的发生装置,反应的化学方程式为:
Ca(ClO)2+4HCl(浓)═CaCl2+2Cl2↑+2H2O.
据此回答下列问题:
(1)装置B中饱和食盐水的作用是除去Cl2中的HCl.
(2)装置B也是安全瓶,目的是监测实验进行时装置C中是否发生堵塞,请写出装置C中发生堵塞时装置B中的实验现象:B中长颈漏斗中液面上升.
(3)装置C的目的是验证氯气是否具有漂白性,则装置C中Ⅰ、Ⅱ、Ⅲ处依次应放入的物质是d(填序号).
| 编号 | I | II | III |
| a | 干燥的有色布条 | 碱石灰 | 湿润的有色布条 |
| b | 干燥的有色布条 | 无水硫酸铜 | 湿润的有色布条 |
| c | 湿润的有色布条 | 浓硫酸 | 干燥的有色布条 |
| d | 湿润的有色布条 | 无水氯化钙 | 干燥的有色布条 |
(5)若所用浓盐酸的浓度为10mol/L,求产生2.24L(标准状况)Cl2时,发生反应的盐酸为40mL.
5.实验室除去硝基苯中的氮氧化物杂质时用不到的仪器是( )
| A. | 漏斗 | B. | 分液漏斗 | C. | 烧杯 | D. | 铁架台 |
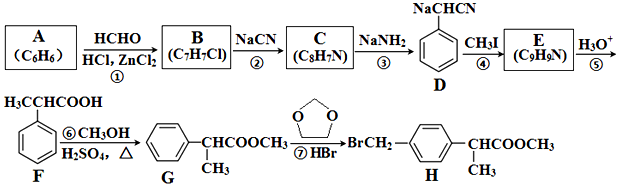
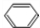 +HCHO+HCl $\stackrel{ZnCl_{2}}{→}$
+HCHO+HCl $\stackrel{ZnCl_{2}}{→}$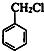 +H2O;反应⑥的化学方程式为
+H2O;反应⑥的化学方程式为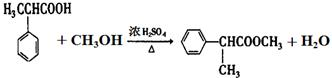 .
.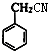 ;E的结构简式为
;E的结构简式为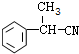 .
. .
.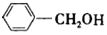 合成
合成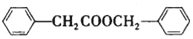 的合成
的合成 .
.