题目内容
下列图象表达正确的是( )
A、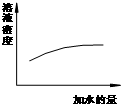 浓硫酸的稀释 |
B、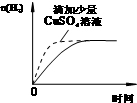 等量的盐酸与过量的锌粉反应 |
C、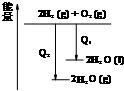 氢气与氧气反应中的能量变化 |
D、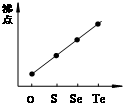 气态氢化物沸点 |
考点:反应热和焓变
专题:图示题
分析:A、浓硫酸加水稀释密度减小;
B、形成原电池可加快化学反应速率,氢气的质量由锌粉的质量决定;
C、物质的燃烧是放热的,液态水变为气态水需要吸收热量;
D、氧族元素的氢化物由于相对分子质量逐渐增大,分子间作用力变大,沸点升高,但其中H2O存在分子间氢键,使其沸点比其他的高很多,总体趋势应是沸点先降低后升高;
B、形成原电池可加快化学反应速率,氢气的质量由锌粉的质量决定;
C、物质的燃烧是放热的,液态水变为气态水需要吸收热量;
D、氧族元素的氢化物由于相对分子质量逐渐增大,分子间作用力变大,沸点升高,但其中H2O存在分子间氢键,使其沸点比其他的高很多,总体趋势应是沸点先降低后升高;
解答:
解:A、浓硫酸加水稀释密度减小,图象与实际不相符,故A错误;
B、锌粉与硫酸铜反应生成了铜,消耗了锌粉,锌粉、铜和盐酸构成了原电池,加快了化学反应速率,锌是足量的,产生的氢气相同,图象与实际相符,故B正确;
C、氢气的燃烧是放热的,但是液态水变为气态水需要吸收热量,所以氢气燃烧生成液态水放出的热量多,故C错误;
D、氧族元素的氢化物由于相对分子质量逐渐增大,分子间作用力变大,沸点升高,但其中H2O存在分子间氢键,使其沸点比其他的高很多,总体趋势应是沸点先降低后升高,故D错误;
故选B.
B、锌粉与硫酸铜反应生成了铜,消耗了锌粉,锌粉、铜和盐酸构成了原电池,加快了化学反应速率,锌是足量的,产生的氢气相同,图象与实际相符,故B正确;
C、氢气的燃烧是放热的,但是液态水变为气态水需要吸收热量,所以氢气燃烧生成液态水放出的热量多,故C错误;
D、氧族元素的氢化物由于相对分子质量逐渐增大,分子间作用力变大,沸点升高,但其中H2O存在分子间氢键,使其沸点比其他的高很多,总体趋势应是沸点先降低后升高,故D错误;
故选B.
点评:本题考查了物质结构和性质的理解应用,注意氢键的形成,原电池原理的分析判断,掌握基础是关键,题目较简单.

练习册系列答案
 优学名师名题系列答案
优学名师名题系列答案
相关题目
同主族元素所形成的同一类化合物,往往其结构和性质相似.化合物PH4I是一种无色晶体,下列对它的描述错误的是( )
| A、是一种共价化合物 |
| B、可由PH3与HI化合生成 |
| C、在加热的条件下,可以分解产生有色气体 |
| D、能跟碱反应放出PH3 |
设NA表示阿伏加德罗常数的数值,下列说法正确的是( )
| A、1 mol NaHSO4晶体中离子总数为2NA |
| B、4.4 g 14CO2含中子数为2.4NA |
| C、0.1 L 3 mol?L-1的NH4NO3溶液中含有的NH4+数目为0.3NA |
| D、1 mol Fe在氧气中充分燃烧失去的电子数为3NA |
下列根据反应原理设计的应用,不正确的是( )
| A、CO32-+H2O?HCO3-+OH- Na2CO3与Al2(SO4)3溶液混合作灭火剂 |
| B、Al3++3H2O?Al(OH)3+3H+ 明矾净水 |
| C、TiCl4+(x+2)H2O(过量)?TiO2?xH2O↓+4HCl 制备TiO2纳米粉 |
| D、SnCl2+H2O?Sn(OH)Cl↓+HCl 配制氯化亚锡溶液时加入浓盐酸 |
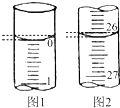 某学生欲用已知物质的量浓度的盐酸来测定未知物质的量浓度的氢氧化钠溶液,请填写下列空白:
某学生欲用已知物质的量浓度的盐酸来测定未知物质的量浓度的氢氧化钠溶液,请填写下列空白: