题目内容
16.酸雨是因为过度燃烧煤和石油制品时,生成硫的氮的氧化物溶于雨水生成硫硫酸和硝酸的缘故.某次酸雨分析数据如下:c(NH4+)=2×10-5mol/L,c(Cl-)=7×10-5mol/L,c(SO42-)=2.8×10-5mol/L c(NO3-)=2.4×10-5mol/L c(Na+)=3×10-5mol/L,据此计算此次酸雨的pH大约为( )| A. | 6 | B. | 5 | C. | 4 | D. | 3 |
分析 溶液中一定满足电荷守恒,根据溶液中电荷守恒计算酸雨中氢离子浓度,然后根据pH的计算公式pH=-lg[H+]计算该酸雨的pH,注意酸雨中的氢氧根离子可以忽略不计.
解答 解:溶液中阴阳离子所带电荷相等,设氢离子浓度为c,氢氧根离子可以忽略不计,
则:[NH4+]+[Na+]+[H+]=[NO3-]+2×[SO42-]+[Cl-],
即:2×10-5mol/L+3×10-5mol/L+c=2.4×10-5mol/L+2×2.8×10-5mol/L+7×10-5mol/L,
解得:c=10-4mol/L,
则该酸雨的pH=-lg10-4=4,
故选C.
点评 本题考查了溶液的pH的简单计算,题目难度不大,明确溶液中阴阳离子所带电荷相等是解本题的关键,注意掌握溶液酸碱性与溶液pH的关系及计算方法.

练习册系列答案
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案
相关题目
6.下列说法正确的是( )
| A. | 氯气溶于水后得到的溶液叫做氯水或液氯 | |
| B. | 次氯酸不稳定,见光易分解出氯气 | |
| C. | 反应Cl2+H2O=HCl+HClO中,H2O是还原剂 | |
| D. | 漂白粉属于混合物 |
7.下列说法正确的是( )
| A. | 常温下,1mol•L-1的弱酸HX的电离度为0.3%,2.0mol•L-1的弱酸HY的电离度为0.5%,由此可知HX比HY弱 | |
| B. | 物质的量浓度相同的H2SO4、NaOH溶液,分别从室温加热到80℃(假设不考虑水的蒸发),溶液的pH均不变 | |
| C. | 由于I2(aq)+I-(aq)?I3-(aq),所以碘单质在KI溶液中的溶解度比在纯水中的大,依此类推Cl2在一定浓度的NaCl溶液中溶解度也比纯水中的大 | |
| D. | 浓度均为0.1mol•L-1的NaClO、NaHCO3溶液的pH分别为10.3和9.7,可说明水解能力HCO3->ClO- |
11.短周期元素W、X、Y、Z原子序数依次增大.X是原子半径最大的短周期元素.Y原子最外层电子数和电子层数,W、Z同主族且原子序数之和与X、Y原子序数之和相等.下列说法中,不正确的是( )
| A. | 含Y元素的盐溶液可呈碱性 | |
| B. | X和W形成的化合物可含非极性共价键 | |
| C. | Y单质与Z的最高价氧化物对应水化物反应一定产生H2 | |
| D. | W的气态氢化物热稳定性强于Z的气态氢化物热稳定 |
8.2002年10月26日,俄罗斯特种部队在解救歌剧院人质时所使用的气体芬太奴,是医疗中使用的一种速效强力镇痛药.它可以通过抑制呼吸和血液循环进行止痛,使人感觉麻木,大量使用能使人昏谜乃至死亡.芬太奴的结构简式为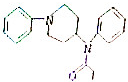 下列关于芬太奴的说法正确的是( )
下列关于芬太奴的说法正确的是( )
 下列关于芬太奴的说法正确的是( )
下列关于芬太奴的说法正确的是( )| A. | 芬太奴的分子式为C20H23N2O | |
| B. | 该分子中所有原子可以共平面 | |
| C. | 芬太奴属于苯的同系物 | |
| D. | 芬太奴在一定条件下可发生水解反应 |