题目内容
18.向等物质的量浓度的盐酸和NH4Cl混合溶液中逐滴加入NaOH溶液(加热),反应过程中,下列离子方程式与事实不相符的是( )| A. | H++OH-═H2O | B. | H++NH4++2OH-═NH3↑+2H2O | ||
| C. | 4H++NH4++5OH-═NH3↑+5H2O | D. | H++2NH4++3OH-═2NH3↑+3H2O |
分析 NaOH不足,先与HCl反应,后来与NH4Cl反应,均与NaOH以1:1反应,并结合溶液中溶质等物质的量浓度判断.
解答 解:A.NaOH少量时,发生H++OH-═H2O,故A正确;
B.NaOH足量,二者均反应时,发生H++NH4++2OH-═NH3↑+2H2O,故B正确;
C.NaOH使盐酸完全反应,使氯化铵部分反应时,发生4H++NH4++5OH-═NH3↑+5H2O,故C正确;
D.等物质的量浓度的盐酸和NH4Cl混合溶液,H++2NH4++3OH-═2NH3↑+3H2O不成立,违反中和的先后顺序,故D错误;
故选D.
点评 本题考查离子反应方程式书写的正误判断,为高频考点,把握反应的先后顺序为解答的关键,侧重分析与应用能力的考查,注意离子反应中保留化学式的物质,题目难度不大.

练习册系列答案
相关题目
19.下列说法中正确的是( )
| A. | 干冰、浓硫酸都是电解质 | |
| B. | Na2O2晶体中既含有离子键又含有共价键 | |
| C. | CaO,Fe2O3、Al2O3既属于碱性氧化物,又属于离子化合物 | |
| D. | 含同一元素的不同化合物,该元素的化合价越高,其氧化性越强 |
20.下列说法不正确的是( )


| A. | 用蘸过蒸馏水的玻璃棒蘸取硫酸钠溶液测其pH,不产生误差 | |
| B. | 称量氢氧化钠固体时,可以直接放在纸上称量 | |
| C. | 沾到试管上的银镜可用稀HNO3洗涤 | |
| D. | 如图可用于吸收HCl气体并防倒吸 |
6.下列关于钠及其化合物的叙述中错误的是( )
| A. | 碳酸钠比碳酸氢钠的热稳定性要好 | |
| B. | 钠在空气中燃烧生成Na2O | |
| C. | 钠在发生化学反应时只作还原剂 | |
| D. | 钠单质暴露在空气中最终将变成Na2CO3 |
3.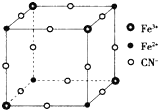 有一种蓝色晶体[可表示为:MFey(CN)6],经X射线研究发现,它的结构特征是Fe3+和Fe2+互相占据立方体互不相邻的顶点,而CN-位于立方体的棱上.其晶体中阴离子的最小结构单元如图所示.下列说法错误的是( )
有一种蓝色晶体[可表示为:MFey(CN)6],经X射线研究发现,它的结构特征是Fe3+和Fe2+互相占据立方体互不相邻的顶点,而CN-位于立方体的棱上.其晶体中阴离子的最小结构单元如图所示.下列说法错误的是( )
 有一种蓝色晶体[可表示为:MFey(CN)6],经X射线研究发现,它的结构特征是Fe3+和Fe2+互相占据立方体互不相邻的顶点,而CN-位于立方体的棱上.其晶体中阴离子的最小结构单元如图所示.下列说法错误的是( )
有一种蓝色晶体[可表示为:MFey(CN)6],经X射线研究发现,它的结构特征是Fe3+和Fe2+互相占据立方体互不相邻的顶点,而CN-位于立方体的棱上.其晶体中阴离子的最小结构单元如图所示.下列说法错误的是( )| A. | 该晶体的化学式为MFe2(CN)6 | |
| B. | 该晶体熔融可导电,且属于化学变化 | |
| C. | 该晶体属于离子晶体,M呈+2价 | |
| D. | 晶体中与每个Fe3+距离最近且等距离的CN-为6个 |
10.下列叙述正确的是( )
| A. | 乙醇汽油是在汽油中加入适量乙醇而形成的一种燃料,它是一种新型化合物 | |
| B. | 用酸性KMnO4溶液不能鉴别CH3CH2CH2CH2OH和CH3CH2CH2COOH | |
| C. | 实验室中提纯混有少量乙酸的乙醇,可采用先加生石灰,过滤后再蒸馏的方法 | |
| D. | 能说明苯不是单双键交替结构的事实是:苯的间二溴代物无同分异构体 |
7.下列除去杂质的方法正确的是( )
| A. | 除去乙烷中少量的乙烯:通过酸性KMnO4溶液进行分离 | |
| B. | 除去乙酸乙酯中少量的乙酸:用饱和氢氧化钠溶液洗涤、分液、干燥、蒸馏 | |
| C. | 除去CO2中少量的HCl气体:气体通过盛饱和碳酸钠溶液的洗气瓶 | |
| D. | 除去乙醇中少量的乙酸:加足量生石灰,蒸馏 |
8.合金具有优良的机械性能,用途广泛.下列物质属于合金的是( )
| A. | 铝 | B. | 青铜 | C. | 石英 | D. | 金刚石 |