题目内容
3.NA是阿伏加德罗常数的值,下列叙述正确的是( )| A. | 1.00mol NaCl中含有NA个NaCl分子 | |
| B. | 1.00mol NaCl中,所有Na+的最外层电子总数为8NA | |
| C. | 欲配制1.00L,1.00mol•L-1的NaCl溶液,可将58.5g NaCl溶于1.00L水中 | |
| D. | 标准状况下,11.2LCH3CH2OH中含有分子的数目为0.5NA |
分析 A.氯化钠为离子晶体;
B.钠离子是原子失去最外层电子形成,离子最外层电子数是8;
C.溶液的体积大于1L;
D.标况下,乙醇为液体.
解答 解:A.氯化钠为离子晶体,不存在分子,故A错误;
B.Na+的最外层电子电子为8,所以1.00 mol NaCl中,所有Na+的最外层电子总数为8mol,最外层电子总数为8NA,故B正确;
C.将58.5g NaCl溶于1.00L水,溶液的体积大于1L,溶液的浓度小于1.00mol•L-1,故C错误;
D.标况下,乙醇为液体,不能使用气体摩尔体积,故D错误;
故选:B.
点评 本题考查了阿伏伽德罗常数的应用,熟悉物质的量的有关计算公式,明确气体摩尔体积适用对象和使用条件是解题关键,题目难度不大.

练习册系列答案
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案
相关题目
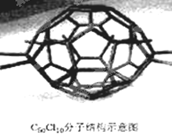
13.厦门大学郑兰荪院士合成了C70Cl10富勒烯足球状分子,如图,它是由C70分子与Cl2发生加成反应得到的.在C70分子中每个碳原子均与周围相邻的其他3个碳原子相连,70个碳原子组成若干个正六边形和正五边形.则有关说法中不正确的是
( )
( )

| A. | C70的熔点比石墨的熔点低 | |
| B. | C70和金刚石是同素异形体 | |
| C. | C70分子中含有70个σ键,35个π键 | |
| D. | C70Cl10分子中共用电子对数目为145个 |
14.用丙醛(CH3-CH2-CHO)制取聚丙烯的过程中发生的反应类型为( )
①取代 ②消去 ③加聚 ④缩聚 ⑤氧化 ⑥还原.
①取代 ②消去 ③加聚 ④缩聚 ⑤氧化 ⑥还原.
| A. | ⑥②③ | B. | ⑤②③ | C. | ②④⑤ | D. | ①④⑥ |
11.元素周期表中某区域可以寻找制备新型农药材料的元素,它们是( )
| A. | 左下方区域的金属元素 | |
| B. | 右上方区域的某些非金属元素 | |
| C. | 金属元素和非金属元素分界线附近的元素 | |
| D. | 过渡元素区域 |
14.二十世纪化学合成技术的发展对人类健康水平和生活质量的提高做出了巨大贡献.下列各组物质全部由化学合成得到的是( )
| A. | 玻璃 纤维素 青霉素 | B. | 石英 橡胶 磷化铟尿素 | ||
| C. | 食盐 聚乙烯 | D. | 涤纶 洗衣粉 阿司匹林 |
 已知A、B、C、D、E都是元素周期表中前四周期的元素,它们的核电荷数A<B<C<D<E.B原子的p轨道半充满,形成的氢化物的沸点是同主族元素的氢化物中最低的.D原子得到一个电子后3p轨道全充满.A+比D原子形成的离子少一个电子层.C与A形成A2C型离子化合物.E的原子序数为26,E原子或离子外围有较多能量相近的空轨道而能与一些分子或离子形成配合物.请根据以上情况,回答下列问题:(答题时,A、B、C、D、E用所对应的元素符号表示)
已知A、B、C、D、E都是元素周期表中前四周期的元素,它们的核电荷数A<B<C<D<E.B原子的p轨道半充满,形成的氢化物的沸点是同主族元素的氢化物中最低的.D原子得到一个电子后3p轨道全充满.A+比D原子形成的离子少一个电子层.C与A形成A2C型离子化合物.E的原子序数为26,E原子或离子外围有较多能量相近的空轨道而能与一些分子或离子形成配合物.请根据以上情况,回答下列问题:(答题时,A、B、C、D、E用所对应的元素符号表示) .
.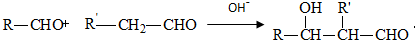 .有机物G(C20H18O4)是一种酯,合成路线如下:
.有机物G(C20H18O4)是一种酯,合成路线如下: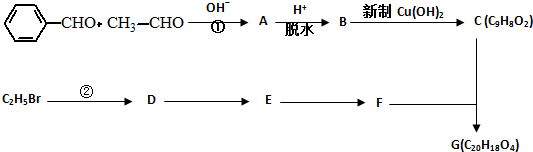
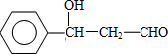 ;F的结构简式:CH2OHCH2OH;
;F的结构简式:CH2OHCH2OH; .
.