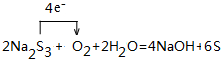题目内容
15.已知: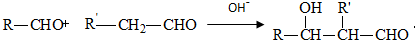 .有机物G(C20H18O4)是一种酯,合成路线如下:
.有机物G(C20H18O4)是一种酯,合成路线如下: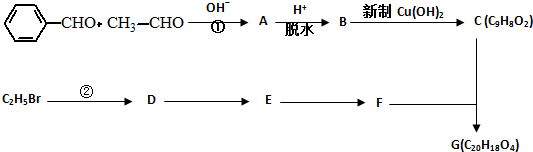
回答下列问题:
(1)指出下列反应类型:反应①加成;反应②消去;
(2)A的结构简式:
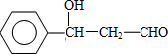 ;F的结构简式:CH2OHCH2OH;
;F的结构简式:CH2OHCH2OH;(3)B转化为C的方程式(用结构简式表示):
 .
.
分析 由题给信息可知A为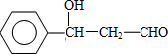 ,脱水可生成B为
,脱水可生成B为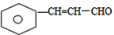 ,B与新制备氢氧化铜反应生成C为
,B与新制备氢氧化铜反应生成C为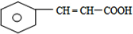 ,由C和G可知F应为CH2OHCH2OH,则D为CH2=CH2,E为CH2BrCH2Br,结合题给信息和有机物的结构和性质解答该题.
,由C和G可知F应为CH2OHCH2OH,则D为CH2=CH2,E为CH2BrCH2Br,结合题给信息和有机物的结构和性质解答该题.
解答 解:由题给信息可知A为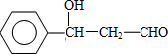 ,脱水可生成B为
,脱水可生成B为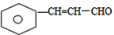 ,B与新制备氢氧化铜反应生成C为
,B与新制备氢氧化铜反应生成C为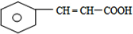 ,由C和G可知F应为CH2OHCH2OH,则D为CH2=CH2,E为CH2BrCH2Br,
,由C和G可知F应为CH2OHCH2OH,则D为CH2=CH2,E为CH2BrCH2Br,
(1)反应①中C=O变成C-O键,应为加成反应,D为CH2=CH2,应由氯代烃发生消去反应生成,
故答案为:加成;消去;
(2)由以上分析可知A的结构简式是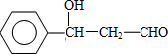 ,F为CH2OHCH2OH,
,F为CH2OHCH2OH,
故答案为: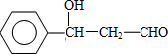 ;CH2OHCH2OH;
;CH2OHCH2OH;
(3)B为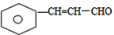 ,与新制备氢氧化铜反应生成C为
,与新制备氢氧化铜反应生成C为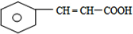 ,反应的方程式为
,反应的方程式为 ,
,
故答案为: ;
;
点评 本题考查有机物的推断,题目难度较大,明确有机物的种类为解答该题的关键,注意结合题给信息结合反应流程中官能团的变化判断.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
5.最近我国接连发生多起煤矿爆炸事故,造成重大人员伤亡和财产损失.煤矿发生爆炸事故的元凶是煤矿坑道气中含有的甲烷.下列关于甲烷的叙述中错误的是( )
| A. | 甲烷分子是一种呈正四面体型的、含极性键的非极性分子 | |
| B. | 甲烷分子中两个氢原子被氯取代后,可形成两种不同结构的分子 | |
| C. | 甲烷是重要的化工原料,其分解产物可用于合成氨和橡胶工业 | |
| D. | “抽”出坑道中的甲烷,既可用作清洁燃料,又可防止爆炸 |
6.某高聚物可表示为: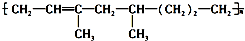 下列有关其叙述不正确的是( )
下列有关其叙述不正确的是( )
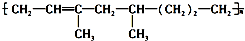 下列有关其叙述不正确的是( )
下列有关其叙述不正确的是( )| A. | 该高聚物是通过加聚反应生成的 | |
| B. | 合成该高聚物的单体有三种 | |
| C. | 1mol该物质能与1molH2加成,生成不含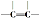 的物质 的物质 | |
| D. | 该高聚物能被酸性KMnO4溶液氧化 |
3.NA是阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 1.00mol NaCl中含有NA个NaCl分子 | |
| B. | 1.00mol NaCl中,所有Na+的最外层电子总数为8NA | |
| C. | 欲配制1.00L,1.00mol•L-1的NaCl溶液,可将58.5g NaCl溶于1.00L水中 | |
| D. | 标准状况下,11.2LCH3CH2OH中含有分子的数目为0.5NA |
20.氰气[(CN)2]和氰化物都是剧毒性物质,氰分子的结构式为N≡C-C≡N,性质与卤素相似,下列叙述错误的是( )
| A. | 氰分子中四原子共直线 | |
| B. | 氰分子中C≡N键长大于C≡C键长 | |
| C. | 氰气分子中含有σ键和π键 | |
| D. | 氰化氢在一定条件下能与烯烃发生加成反应 |
4.汽车尾气中的氮氧化物(NOx)是大气的污染物,不仅可直接导致动植物中毒而且会参与酸雨及光化学烟雾的形成,所以要尽可能的消除.消除方法之一是在汽车排气管中装上催化转化器,利用反应:4xNH3+6NOx═(2x+3)N2+6xH2O使氮氧化物转化为无害物质,在该反应中还原剂与转移电子的数目关系中正确的是( )
| A. | NH3(12e-) | B. | NOx(12e-) | C. | NH3(12xe-) | D. | NOx(12xe-) |
6.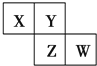 X、Y、Z、W均为短周期元素,在周期表中位置如图,Y原子的最外层电子数是其次外层电子数的3倍.下列说法正确的是( )
X、Y、Z、W均为短周期元素,在周期表中位置如图,Y原子的最外层电子数是其次外层电子数的3倍.下列说法正确的是( )
 X、Y、Z、W均为短周期元素,在周期表中位置如图,Y原子的最外层电子数是其次外层电子数的3倍.下列说法正确的是( )
X、Y、Z、W均为短周期元素,在周期表中位置如图,Y原子的最外层电子数是其次外层电子数的3倍.下列说法正确的是( )| A. | X、Y、Z的原子半径大小:X>Y>Z | |
| B. | Y、Z的气态氢化物中,前者更稳定 | |
| C. | Z、W的最高价氧化物对应水化物的酸性,前者更强 | |
| D. | X、W的气态氢化物相互反应,生成物中只含离子键不含共价键 |
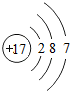 ;
; ,该化合物的水溶液在空气中久置后变质,生成一种单质和一种强碱,用化学方程式表示这一变化过程并用单线桥标记电子转移的方向和数目:
,该化合物的水溶液在空气中久置后变质,生成一种单质和一种强碱,用化学方程式表示这一变化过程并用单线桥标记电子转移的方向和数目: