题目内容
14.用丙醛(CH3-CH2-CHO)制取聚丙烯的过程中发生的反应类型为( )①取代 ②消去 ③加聚 ④缩聚 ⑤氧化 ⑥还原.
| A. | ⑥②③ | B. | ⑤②③ | C. | ②④⑤ | D. | ①④⑥ |
分析 可用逆推法分析: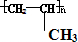 →CH2=CH-CH3→CH2OH-CH2-CH3→CH3-CH2-CHO,以此判断可能发生的反应.
→CH2=CH-CH3→CH2OH-CH2-CH3→CH3-CH2-CHO,以此判断可能发生的反应.
解答 解:要制取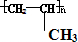 ,可逆推反应流程:
,可逆推反应流程: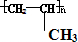 →CH2=CH-CH3→CH2OH-CH2-CH3→CH3-CH2-CHO,则从后往前推断可发生加成(还原)、消去、加聚反应,
→CH2=CH-CH3→CH2OH-CH2-CH3→CH3-CH2-CHO,则从后往前推断可发生加成(还原)、消去、加聚反应,
故选A.
点评 本题考查有机物的合成,题目难度不大,本题注意根据有机物的官能团的变化结合有机物的性质用逆推法判断.

练习册系列答案
 提分百分百检测卷系列答案
提分百分百检测卷系列答案 宝贝计划期末冲刺夺100分系列答案
宝贝计划期末冲刺夺100分系列答案 能考试全能100分系列答案
能考试全能100分系列答案
相关题目
4.下列离子方程式书写错误的是( )
| A. | 向足量的NaHCO3溶液中逐渐滴入澄清石灰水:Ca2++2OH-+2HCO3-═2H2O+CaCO3↓+CO32- | |
| B. | 向足量的NaHSO4溶液中逐渐滴入Ba(HCO3)2溶液:Ba2++2H++2HCO3-+SO42-═2H2O+BaSO4↓+2 CO2↑ | |
| C. | 向饱和Na2CO3溶液中通入足量的CO2:CO32-+CO2+H2O═2HCO3- | |
| D. | 向NaHSO4溶液中逐渐滴入Ba(OH)2溶液至沉淀完全:H++SO42-+Ba2++OH-═BaSO4↓+H2O |
5.最近我国接连发生多起煤矿爆炸事故,造成重大人员伤亡和财产损失.煤矿发生爆炸事故的元凶是煤矿坑道气中含有的甲烷.下列关于甲烷的叙述中错误的是( )
| A. | 甲烷分子是一种呈正四面体型的、含极性键的非极性分子 | |
| B. | 甲烷分子中两个氢原子被氯取代后,可形成两种不同结构的分子 | |
| C. | 甲烷是重要的化工原料,其分解产物可用于合成氨和橡胶工业 | |
| D. | “抽”出坑道中的甲烷,既可用作清洁燃料,又可防止爆炸 |
2.已知aAn+,bB(n+1)+,cCn-,dD(n+1)-是具有相同的电子层结构的短周期元素形成的简单离子,下列叙述正确的是( )
| A. | 最外层电子数:C>D>A>B | B. | 原子序数:b>a>c>d | ||
| C. | 离子半径:Cn->D(n+1)->An+>B(n+1)+ | D. | 单质还原性:B>A>C>D |
9.某反应的反应物与生成物有K2Cr2O7、KCl、CrCl3、Cl2、HCl、H2O,已知氧化性:K2Cr2O7>Cl2,则下列说法不正确的是( )
| A. | 氧化剂和还原剂的物质的量之比为1:14 | |
| B. | 由该反应可知还原性:HCl>CrCl3 | |
| C. | 当转移0.2mol电子时,被氧化的还原剂的物质的量为0.2mol | |
| D. | Cl2是该反应的氧化产物 |
19.下列叙述正确的是( )
| A. | 铜锌稀硫酸形成的原电池放电时,溶液中阳离子向铜电极移动 | |
| B. | 燃料电池在使用时发生了燃料的燃烧 | |
| C. | 增大反应物的用量,反应速率一定加快 | |
| D. | 可逆反应达到一定限度后,因各物质的浓度不变,说明反应已经停止 |
6.某高聚物可表示为: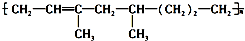 下列有关其叙述不正确的是( )
下列有关其叙述不正确的是( )
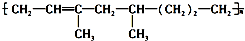 下列有关其叙述不正确的是( )
下列有关其叙述不正确的是( )| A. | 该高聚物是通过加聚反应生成的 | |
| B. | 合成该高聚物的单体有三种 | |
| C. | 1mol该物质能与1molH2加成,生成不含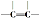 的物质 的物质 | |
| D. | 该高聚物能被酸性KMnO4溶液氧化 |
3.NA是阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 1.00mol NaCl中含有NA个NaCl分子 | |
| B. | 1.00mol NaCl中,所有Na+的最外层电子总数为8NA | |
| C. | 欲配制1.00L,1.00mol•L-1的NaCl溶液,可将58.5g NaCl溶于1.00L水中 | |
| D. | 标准状况下,11.2LCH3CH2OH中含有分子的数目为0.5NA |
4.汽车尾气中的氮氧化物(NOx)是大气的污染物,不仅可直接导致动植物中毒而且会参与酸雨及光化学烟雾的形成,所以要尽可能的消除.消除方法之一是在汽车排气管中装上催化转化器,利用反应:4xNH3+6NOx═(2x+3)N2+6xH2O使氮氧化物转化为无害物质,在该反应中还原剂与转移电子的数目关系中正确的是( )
| A. | NH3(12e-) | B. | NOx(12e-) | C. | NH3(12xe-) | D. | NOx(12xe-) |