题目内容
2.按要求填空:H2O的电子式:
 ; N2结构式:N≡N.
; N2结构式:N≡N.
分析 水为共价化合物,氧原子最外层8个电子,分子中存在两个氧氢键;
氮气分子中两个氮原子各拿出3个电子形成3对共用电子对,形成氮氮三键;
解答 解:水中存在两个氧氢键,氧原子最外层达到8电子稳定结构,水的电子式为 ;
;
氮气分子中存在氮氮三键,氮气的结构式为:N≡N;
故答案为: ;N≡N;
;N≡N;
点评 本题考查了常用化学用语,熟悉电子式、结构式的书写方法,明确水分子含有化学键类型、氮气分子的结构特点是解题关键,题目难度不大.

练习册系列答案
相关题目
13.如图所示的原子结构示意图中,能组成AB2型化合物的是( )
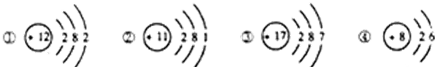
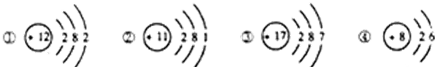
| A. | ①③ | B. | ②④ | C. | ②③ | D. | ①④ |
10.已知四价铅有强氧化性,能跟盐酸反应生成氯气,将SO2通入悬浮着黑色PbO2的热水中,过一会儿,将发生的情形是( )
| A. | 悬浮物由黑色变为白色,因SO2是一种漂白剂 | |
| B. | 悬浮物由黑色变为白色,因为形成了PbSO4 | |
| C. | 有黄色沉淀生成 | |
| D. | 有臭鸡蛋味的气体放出 |
7.某有机物R的结构简式如图所示.下列关于R的说法不正确的是( )
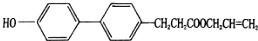

| A. | 能发生加成、加聚、水解和氧化反应 | |
| B. | 分子式为C18H20O3 | |
| C. | 该化合物最多有12个碳原子共平面 | |
| D. | 一定条件下1molR最多可以消耗2molNaoH |
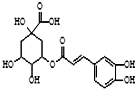 金银花的有效成分为绿原酸,具有广泛的杀菌、消炎功能,其结构简式如图.
金银花的有效成分为绿原酸,具有广泛的杀菌、消炎功能,其结构简式如图.