题目内容
18.下列各组溶液,只用试管和胶头滴管,不用任何试剂就可以鉴别的是( )| A. | NaHCO3 HCl | B. | Na2CO3 HCl | C. | AlCl3 NaOH | D. | CaCl2 Na2CO3 |
分析 只用试管和胶头滴管,不用任何化学试剂就可以鉴别的物质可以采用相互滴加的方法检验,滴加顺序不同,现象不同的可以鉴别.
解答 解:A.盐酸与碳酸氢钠反应的离子方程式为:H++HCO3-=CO2↑+H2O,二者混合后会生成气体,不能通过滴加顺序鉴别,故A错误;
B.Na2CO3溶液滴入盐酸中,立即产生气体,若将盐酸滴入Na2CO3溶液中,开始没有气体生成,后有气体生成,二者显现不同,可鉴别,故B正确;
C.将AlCl3溶液滴入NaOH溶液中,先没有明显现象,后生成白色沉淀,将NaOH溶液滴入AlCl3溶液中,先生成白色沉淀,后白色沉淀溶解,二者显现不同,可鉴别,故C正确;
D.CaCl2 Na2CO3混合反应生成碳酸钙沉淀,不能通过滴加顺序鉴别,故D错误.
故选BC.
点评 本题考查利用滴加顺序不同鉴别物质,题目难度中等,注意滴加顺序不同实质是反应物量的不同,掌握常见与量及顺序有关的反应,注意基础知识的全面掌握.

练习册系列答案
相关题目
8.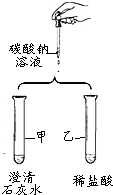 如图是某小组验证碳酸钠性质的实验方案.
如图是某小组验证碳酸钠性质的实验方案.
(1)甲试管中反应的化学方程式为Na2CO3+Ca(OH)2═2NaOH+CaCO3↓;
(2)乙试管中的现象是大量气泡.
实验后他们将废液倒入废液缸,小欣发现废液澄清.
【提出问题】废液中的溶质含有哪些成分?
【查阅资料】①CaCl2溶液呈中性
②CaCl2+Na2CO3═2NaCl+CaCO3↓
【提出猜想】可能是Ⅰ.CaCl2、NaClⅡ.CaCl2、NaCl HCl
【设计实验】验证你的猜想
【讨论】如果废液是浑浊的,过滤后滤液中肯定没有物质是HCl.
 如图是某小组验证碳酸钠性质的实验方案.
如图是某小组验证碳酸钠性质的实验方案.(1)甲试管中反应的化学方程式为Na2CO3+Ca(OH)2═2NaOH+CaCO3↓;
(2)乙试管中的现象是大量气泡.
实验后他们将废液倒入废液缸,小欣发现废液澄清.
【提出问题】废液中的溶质含有哪些成分?
【查阅资料】①CaCl2溶液呈中性
②CaCl2+Na2CO3═2NaCl+CaCO3↓
【提出猜想】可能是Ⅰ.CaCl2、NaClⅡ.CaCl2、NaCl HCl
【设计实验】验证你的猜想
| 实验步骤 | 实验现象 | 结论 |
| 取少量的废液于试管中,滴加2~3滴石蕊试液,振荡. | 无现象 | 废液的pH=7; 猜想Ⅰ成立. |
6.下列有关化学与生活、技术的说法中不正确的是( )
| A. | 考古时可用12C测定一些文物的年代 | |
| B. | 可在元素周期表的过渡元素中寻找催化剂和耐高温、耐腐蚀的合金材料 | |
| C. | 乙烯是一种重要的基本化工原料,它的产量可以用来衡量一个国家的石油化工发展水平 | |
| D. | 红葡萄酒的密封储存时间越长,质量越好,原因之一是储存过程中生成了有香味的酯 |
3.下列关于氧化物的叙述中,正确的是( )
| A. | 酸性氧化物都可以与强碱溶液反应 | |
| B. | 与水反应生成酸的氧化物都是酸性氧化物 | |
| C. | 金属氧化物都是碱性氧化物或两性氧化物 | |
| D. | 不能与酸反应的氧化物一定能与碱反应 |
10.由A、B、C、D四种金属按表中装置进行实验.
根据实验现象回答下列问题:
①装置乙中正极的电极反应式是Cu2++2e-═Cu.
②四种金属活动性由强到弱的顺序是D>A>B>C.
| 装置 | 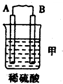 | 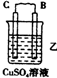 |  |
| 现象 | 二价金属A不断溶解 | C的质量增加 | A上有气体产生 |
①装置乙中正极的电极反应式是Cu2++2e-═Cu.
②四种金属活动性由强到弱的顺序是D>A>B>C.
7.某烃甲与氢气反应后的产物乙为(CH3)2CHCH2CH3,则相关说法不合理的是( )
| A. | 产物乙的系统命名为2-甲基丁烷 | |
| B. | 烃甲可能是2-甲基-1,3-丁二烯 | |
| C. | 0.1 mol产物乙完全燃烧可消耗17.92L O2 | |
| D. | 烃甲与乙炔可能是同系物 |
8.往NaOH溶液中加入少量的稀醋酸,若温度不变,下列数据一定不变的是( )
| A. | 溶液的质量 | B. | 水的离子积 | C. | OH-物质的量浓度 | D. | 溶液pH值 |
