题目内容
3.设NA表示阿伏加德罗常数的值,下列说法正确的是( )| A. | 标准状况下,22.4L SO3中含有氧原子数目为3NA | |
| B. | 常温常压下,56g铁与足量硫粉反应,转移的电子数目为3NA | |
| C. | 标准状况下,22.4L Cl2溶于足量水中,转移的电子数目为NA | |
| D. | 标准状况下,22.4L NH3溶于水配成1L溶液,其浓度为1mol/L |
分析 A、标况下三氧化硫为固体;
B、求出铁的物质的量,然后根据铁和硫反应后变为+2价来分析;
C、氯气和水的反应为可逆反应;
D、求出氨气的物质的量,然后根据物质的量浓度c=$\frac{n}{V}$来计算.
解答 解:A、标况下三氧化硫为固体,故不能根据气体摩尔体积来计算其物质的量和含有的氧原子个数,故A错误;
B、56g铁的物质的量为1mol,而铁和硫反应后变为+2价,故1mol铁转移2NA个电子故B错误;
C、氯气和水的反应为可逆反应,不能进行彻底,故转移的电子数小于NA个,故C错误;
D、标况下22.4L氨气的物质的量为1mol,溶于水后所得溶液的物质的量浓度c=$\frac{n}{V}$=$\frac{1mol}{1L}$=1mol/L,故D正确.
故选D.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 全能测控期末小状元系列答案
全能测控期末小状元系列答案
相关题目
12.在0.1mol/L NaHSO3溶液中存在着微粒浓度的关系式,正确的是( )
| A. | c(Na+)>c(HSO3-)>c(SO32-)>c(H+)>c(OH-) | B. | c(Na+)+c(H+)=c(HSO3-)+c(SO32-)+c(OH-) | ||
| C. | c(H2SO3)+c(H+)=c(SO32-)+c(OH-) | D. | c(Na+)=c(HSO3-)+2c(SO32-)+c(H2SO3) |
8.化学与生活密切相关,下列说法中正确的是( )
| A. | “歼-20”飞机上使用的碳纤维是一种新型的有机高分子材料 | |
| B. | 工业上通常用电解Na、Mg、Al对应的氯化物制取三种金属单质 | |
| C. | 燃料电池中燃料都是在负极发生氧化反应 | |
| D. | Fe3O4俗称铁红,常作红色油漆和涂料 |
15.下列实验正确的是 ( )
| A. | 取少量溶液滴加Ca(OH)2溶液,观察是否出现白色浑浊,确定NaHCO3溶液中是否混有Na2CO3 | |
| B. | 苯酚沾到皮肤上,先用酒精清洗,再用水冲洗 | |
| C. | 将10g ZnSO4•7H2O溶解在90g水中,配制10%ZnSO4溶液 | |
| D. | 向稀硫酸中加几滴CuSO4溶液,可提高纯锌与稀硫酸的反应速率. |
12.下列有关描述及离子方程式的书写正确的是( )
| A. | HSO3-在溶液中发生水解:HSO3-+H2O?SO32-+H3O+ | |
| B. | 向Mg(OH)2浊液中滴加FeCl3溶液生成红褐色沉淀:3OH-+Fe3+=Fe(OH)3↓ | |
| C. | 碳酸氢钠溶液显碱性:HCO3-+H2O?H2CO3+OH- | |
| D. | 惰性电极电解MgCl2溶液:Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$OH-+Cl2↑+H2↑ |
13.下列有关有机物的性质和用途的说法正确的是( )
| A. | 乙烯分子与苯分子中碳碳键不同,但二者都能发生加成反应 | |
| B. | 乙烯、聚氯乙烯、苯乙烯分子结构中都含有不饱和键 | |
| C. | 乙醇既可以作燃料,也可以在日常生活中使用,如无水乙醇可用于杀菌、消毒、漂白 | |
| D. | 石油的分馏、裂化和煤的干馏都是化学变化 |
 W、X、Y、Z、M、Q均为稀有气体外的短周期元素,其原子序数依次增大,X的最外层电子数是W的电子总数的4倍,Z与M最外层电子数相同,X与M在周期表中的位置如图:
W、X、Y、Z、M、Q均为稀有气体外的短周期元素,其原子序数依次增大,X的最外层电子数是W的电子总数的4倍,Z与M最外层电子数相同,X与M在周期表中的位置如图: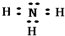 .
.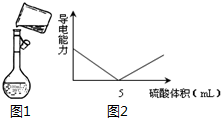 用98%的浓硫酸(密度为1.84g/mL)配制500mL 0.30mol/L 稀硫酸的实验步骤如下:①计算所用浓硫酸的体积;②量取一定体积的浓硫酸;③稀释;④冷却,转移、洗涤摇匀;⑤定容、摇匀;⑥转入试剂瓶,贴标签.
用98%的浓硫酸(密度为1.84g/mL)配制500mL 0.30mol/L 稀硫酸的实验步骤如下:①计算所用浓硫酸的体积;②量取一定体积的浓硫酸;③稀释;④冷却,转移、洗涤摇匀;⑤定容、摇匀;⑥转入试剂瓶,贴标签.