题目内容
12.下列有关描述及离子方程式的书写正确的是( )| A. | HSO3-在溶液中发生水解:HSO3-+H2O?SO32-+H3O+ | |
| B. | 向Mg(OH)2浊液中滴加FeCl3溶液生成红褐色沉淀:3OH-+Fe3+=Fe(OH)3↓ | |
| C. | 碳酸氢钠溶液显碱性:HCO3-+H2O?H2CO3+OH- | |
| D. | 惰性电极电解MgCl2溶液:Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$OH-+Cl2↑+H2↑ |
分析 A、HSO3-在溶液中水解为H2SO3;
B、氢氧化镁是弱碱,不能拆;
C、HCO3-在溶液中发生水解显碱性;
D、电解氯化镁溶液时,氯离子在阳极放电,来自于水的氢离子在阳极放电.
解答 解:A、HSO3-在溶液中水解为H2SO3,故水解的离子方程式为:HSO3-+H2O?H2SO3+OH-,故A错误;
B、氢氧化镁是弱碱,不能拆,故正确的离子方程式为,故向Mg(OH)2浊液中滴加FeCl3溶液生成红褐色沉淀的离子方程式为:3Mg(OH)2+2Fe3+=2Fe(OH)3↓+3Mg2+,故B错误;
C、HCO3-在溶液中发生水解显碱性,HCO3-+H2O?H2CO3+OH-,故C正确;
D、电解氯化镁溶液时,氯离子在阳极放电,来自于水的氢离子在阳极放电,生成氢氧化镁沉淀,故离子方程式为:Mg2++2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$Mg(OH)2↓+Cl2↑+H2↑,故D错误.
故选C.
点评 本题考查了离子方程式的书写,难度不大,应注意的是电离方程式和水解方程式的区别.

练习册系列答案
 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案
相关题目
3.设NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 标准状况下,22.4L SO3中含有氧原子数目为3NA | |
| B. | 常温常压下,56g铁与足量硫粉反应,转移的电子数目为3NA | |
| C. | 标准状况下,22.4L Cl2溶于足量水中,转移的电子数目为NA | |
| D. | 标准状况下,22.4L NH3溶于水配成1L溶液,其浓度为1mol/L |
20.下列电解质在水溶液中和熔化状态下均能导电的是( )
| A. | 硫酸 | B. | 碳酸钙 | C. | 氢氧化钠 | D. | 氧化镁 |
7.11.6gFe3O4加到100mL某浓度的盐酸中,再加入9.8g铁粉,反应停止时,溶液中无固体存在.向溶液中滴加硫氰化钾溶液,未见颜色变化,为了中和过量的盐酸(不考虑盐酸的挥发),且使铁完全转化成Fe(OH)2,共消耗5.0mol•L-1NaOH溶液160mL.则原盐酸的物质的量浓度为( )
| A. | 2 mol•L-1 | B. | 4 mol•L-1 | C. | 6 mol•L-1 | D. | 8 mol•L-1 |
17.若NA表示阿伏加德罗常数,下列说法中正确的是( )
| A. | 在密闭容器中加入3mol H2和1molN2,充分反应后可得到NH3分子数为2NA | |
| B. | 0.1mol/L Na2SO4溶液中含有Na+为0.2NA | |
| C. | 一定条件下,23 g Na与O2反应生成Na2O2时失去的电子数为NA | |
| D. | 标准状况下,22.4L SO3中含有的氯原子数为3NA |
4.某气体的摩尔质量为Mg/mol NA表示阿伏伽德罗常数的值,在一定温度和压强下,体积为VL的该气体所含的分子数为x,MX/VNA表示的是( )
| A. | 以为单位1L 该气体的质量 | B. | 以“克”为单位,VL该气体的质量 | ||
| C. | 1L该气体中所含的分子数 | D. | 以“升”为单位 1mol该气体的体积 |
2.结构简式为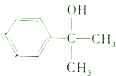 的有机物在一定条件下能和氢气完全加成,加成产物的一溴代物有(不考虑-OH的取代)( )
的有机物在一定条件下能和氢气完全加成,加成产物的一溴代物有(不考虑-OH的取代)( )
 的有机物在一定条件下能和氢气完全加成,加成产物的一溴代物有(不考虑-OH的取代)( )
的有机物在一定条件下能和氢气完全加成,加成产物的一溴代物有(不考虑-OH的取代)( )| A. | 4种 | B. | 5种 | C. | 6种 | D. | 7种 |
 水是一种重要的自然资源,是人类赖以生存不可缺少的物质.请回答下列问题:
水是一种重要的自然资源,是人类赖以生存不可缺少的物质.请回答下列问题: