题目内容
14.甲醇来源丰富、价格低廉,是一种重要的化工原料,有着重要的应用前景.(1)工业上以CH4和H2O为原料,通过下列反应来制备甲醇:
I:CH4 ( g )+H2O ( g )=CO ( g )+3H2 ( g )△H=+206.0kJ•mol-1
II:CO ( g )+2H2 ( g )=CH3OH ( g )△H=-129.0kJ•mol-1
CH4(g)与H2O(g)反应生成CH3OH (g)和H2(g)的热化学方程式为CH4(g)+H2O(g)=CH3OH (g)+H2 (g)△H=+77.0 kJ/mol.
(2)若以CH4、CO和H2O(g)为原料制备甲醇,欲使原子利用率最高,则投料时n(CH4):n(CO):n(H2O)是2:1:2.
(3)若在恒温恒容的容器内进行反应:CO(g)+2H2(g)?CH3OH(g),该反应平衡常数表达式为K=$\frac{c(C{H}_{3}OH)}{c(CO).{c}^{2}({H}_{2})}$.一定条件下,可用来判断该反应达到平衡状态的标志有AD.(填字母)
A.CO百分含量保持不变
B.容器中H2浓度与CO浓度相等
C.容器中混合气体的密度保持不变
D.CO的生成速率与CH3OH的生成速率相等
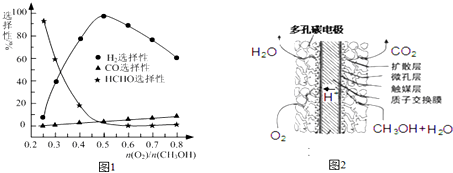
(4)工业上利用甲醇部分氧化制备氢气.在一定温度和催化剂作用下,原料气比例对反应的选择性(选择性越大,表示生成的该物质越多)影响关系如图1所示.则在制备H2时发生的主要反应方程式为2CH3OH+O2$→_{△}^{催化剂}$ 2CO2+4H2(已知产物为两种气体);n(O2):n(CH3OH)=0.25时,主要产物为HCHO.
(5)甲醇燃料电池结构如图2所示.其工作时负极电极反应式可表示为:CH3OH-6e-+H2O=CO2↑+6H+.
分析 (1)Ⅰ、CH4(g)+H2O(g)=CO(g)+3H2(g)△H=+206.0kJ/mol
Ⅱ、CO(g)+2 H2(g)=CH3OH(g)△H=-129.0 kJ/mol
根据盖斯定律将方程式Ⅰ+Ⅱ计算得到;
(2)要使原子利用率最高,则应该产物中只有甲醇,
I:CH4+H2O=CO+3H2
II:CO+2H2=CH3OH
将方程式I×2+II×3得2CH4+2H2O+CO=3CH3OH,据此判断三种物质的物质的量之比;
(3)该平衡常数K等于生成物浓度幂之积与反应物浓度幂之积的比;可逆反应达到平衡状态时,正逆反应速率相等,反应体系中各物质的物质的量、物质的量浓度、百分含量及由此引起的一系列物理量不变;
(4)根据图知,氢气的选择性较大,说明生成氢气,CO的选择性几乎不变,说明没有二氧化碳生成,甲醇被氧化生成两种气体,则另外一种应该是二氧化碳;n(O2):n(CH3OH)=0.25时,其主要产物是甲醛;
(5)甲醇燃料酸性电池中,加入甲醇的电极是负极,负极上甲醇失电子生成二氧化碳和氢离子.
解答 解:(1)Ⅰ、CH4(g)+H2O(g)=CO(g)+3H2(g)△H=+206.0kJ/mol
Ⅱ、CO(g)+2 H2(g)=CH3OH(g)△H=-129.0 kJ/mol
将方程式Ⅰ+Ⅱ得CH4(g)+H2O(g)=CH3OH(g)+H2(g)△H=+206.0kJ/mol+(-129.0kJ/mol)=+77.0 kJ/mol,故答案为:CH4 ( g )+H2O ( g )=CH3OH ( g )+H2 ( g )△H=+77.0 kJ•mol-1;
(2)要使原子利用率最高,则应该产物中只有甲醇,
I:CH4+H2O=CO+3H2
II:CO+2H2=CH3OH
将方程式I×2+II×3得2CH4+2H2O+CO=3CH3OH,根据方程式知,n(CH4):n(CO):n(H2O)=2:1:2,
故答案为:2:1:2;
(3)该平衡常数K等于生成物浓度幂之积与反应物浓度幂之积的比,则该平衡常数K=$\frac{c(C{H}_{3}OH)}{c(CO).{c}^{2}({H}_{2})}$;
A.CO百分含量保持不变时,正逆反应速率相等,该反应达到平衡状态,故正确;
B.容器中H2浓度与CO浓度相等,该反应不一定达到平衡状态,与反应物初始浓度及转化率有关,故错误;
C.反应前后气体总质量不变、容器容积不变,则无论反应是否达到平衡状态,容器中混合气体密度始终不变,所以当容器中混合气体的密度保持不变时该反应不一定达到平衡状态,故错误;
D.CO的生成速率与CH3OH的生成速率相等也等于消耗的甲醇速率,则该反应达到平衡状态,故正确;
故答案为:K=$\frac{c(C{H}_{3}OH)}{c(CO).{c}^{2}({H}_{2})}$;AD;
(4)根据图知,氢气的选择性较大,说明生成氢气,CO的选择性几乎不变,说明没有二氧化碳生成,甲醇被氧化生成两种气体,则另外一种应该是二氧化碳,其反应方程式为2CH3OH+O2$→_{△}^{催化剂}$ 2CO2+4H2;n(O2):n(CH3OH)=0.25时,根据图知,其主要产物是甲醛,
故答案为:2CH3OH+O2$→_{△}^{催化剂}$ 2CO2+4H2;HCHO;
(5)甲醇燃料酸性电池中,加入甲醇的电极是负极,负极上甲醇失电子生成二氧化碳和氢离子,电极反应式为CH3OH-6e-+H2O=CO2↑+6H+,故答案为:CH3OH-6e-+H2O=CO2↑+6H+.
点评 本题考查较综合,涉及化学平衡计算、原电池原理、化学平衡状态判断、盖斯定律等知识点,为高频考点,侧重考查学生分析计算判断能力,明确化学反应原理是解本题关键,注意教材知识的综合及灵活应用,题目难点中等.

 阅读快车系列答案
阅读快车系列答案| A. | H3O+和OH- | B. | CH3+和NH4+ | C. | NO3-和NO2- | D. | SO42-和PO43- |
| A. | 氯气 二氧化碳 氢氧化钠 | B. | 氯化钠 过氧化钠 氯化铵 | ||
| C. | 氯化钠 过氧化氢 氯化铵 | D. | 氯化钠 氦气 氢氧化钠 |
 铁及其化合物在生产、生活中有广泛应用,如高铁酸钾(K2FeO4)具有极强的氧化性,是一种优良的水处理剂;又知高炉炼铁过程中发生的主要反应为:$\frac{1}{3}$Fe2O3(s)+CO(g)?$\frac{2}{3}$Fe(s)+CO2(g)+Q kJ,下表中是该反应在不同温度下的平衡常数:
铁及其化合物在生产、生活中有广泛应用,如高铁酸钾(K2FeO4)具有极强的氧化性,是一种优良的水处理剂;又知高炉炼铁过程中发生的主要反应为:$\frac{1}{3}$Fe2O3(s)+CO(g)?$\frac{2}{3}$Fe(s)+CO2(g)+Q kJ,下表中是该反应在不同温度下的平衡常数:| 温度/℃ | 1000 | 1115 | 1300 |
| 平衡常数 | 4.0 | 3.7 | 3.5 |
(2)在一个容积为10L的密闭容器中,1000℃时加入Fe、Fe2O3、CO、CO2各1.0mol,此时υ正>υ逆(填“>”、“<”或“=”).经过10min,在1000℃达到平衡,则该时间范围内反应的平均反应速率υ(CO2)=0.006mol/(L•min);
(3)已知:4FeO42-+10H2O?4Fe(OH)3+8OH-+3O2. K2FeO4在处理水的过程中所起的作用有杀菌消毒、净水(吸附悬浮物);
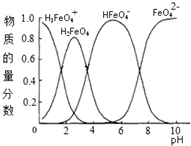
(4)高铁酸钾水溶液中FeO42-的存在形态及它们的物质的量分数随pH的变化如图所示:
(1)pH=2时溶液存在如下等量关系:c(K+)=2c(H2FeO4)+2c(H3FeO4+)+2c(HFeO4-);
(2)向pH=6的溶液中加入KOH溶液,发生反应的离子方程式为HFeO4-+OH-=FeO42-+H2O.
| A. | 标准状况下,22.4L SO3中含有氧原子数目为3NA | |
| B. | 常温常压下,56g铁与足量硫粉反应,转移的电子数目为3NA | |
| C. | 标准状况下,22.4L Cl2溶于足量水中,转移的电子数目为NA | |
| D. | 标准状况下,22.4L NH3溶于水配成1L溶液,其浓度为1mol/L |
| A. | 以为单位1L 该气体的质量 | B. | 以“克”为单位,VL该气体的质量 | ||
| C. | 1L该气体中所含的分子数 | D. | 以“升”为单位 1mol该气体的体积 |
 水是一种重要的自然资源,是人类赖以生存不可缺少的物质.请回答下列问题:
水是一种重要的自然资源,是人类赖以生存不可缺少的物质.请回答下列问题: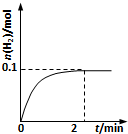 硫-碘循环分解水制氢主要涉及下列反应:
硫-碘循环分解水制氢主要涉及下列反应: