题目内容
已知铜和浓硫酸可以在加热条件下发生如下反应(反应方程式已配平):Cu+2H2SO4(浓)═CuSO4+A↑+2H2O 试通过计算和推理完成下面的问题:
(1)A物质可以导致酸雨的形成.则A应该属于 (填字母代号).
a.酸 b. 碱 c. 盐 d. 酸性氧化物 e. 碱性氧化物
A物质可以使酸性KMnO4溶液褪色,此反应中 (填写化学式)失去电子.
(2)学习了分类法后,甲同学把下列物质分为一类:CuSO4溶液、CuSO4?5H2O、Cu(OH)2、液态O2.你认为甲同学分类的标准是 .根据物质之间的反应关系判断,下列反应能生成CuSO4的是 (用字母代号填写).
a.金属+酸 b. 金属氧化物+酸 c. 碱+酸 d. 盐+酸
(3)将反应后所得到的CuSO4溶液与足量Ba(OH)2溶液充分反应.请写出此过程发生的反应的离子方程式: .
(1)A物质可以导致酸雨的形成.则A应该属于
a.酸 b. 碱 c. 盐 d. 酸性氧化物 e. 碱性氧化物
A物质可以使酸性KMnO4溶液褪色,此反应中
(2)学习了分类法后,甲同学把下列物质分为一类:CuSO4溶液、CuSO4?5H2O、Cu(OH)2、液态O2.你认为甲同学分类的标准是
a.金属+酸 b. 金属氧化物+酸 c. 碱+酸 d. 盐+酸
(3)将反应后所得到的CuSO4溶液与足量Ba(OH)2溶液充分反应.请写出此过程发生的反应的离子方程式:
考点:酸、碱、盐、氧化物的概念及其相互联系,离子方程式的书写
专题:
分析:(1)由质量守恒定律可知反应Cu+2H2SO4(浓)
CuSO4+A↑+2H2O中,A为SO2,是酸性氧化物,可导致酸雨,具有还原性,能被酸性KMnO4溶液氧化;
(2)物质中均含氧元素,Cu与浓硫酸、CuO与硫酸、氢氧化铜与硫酸、氯化钡与硫酸均可生成硫酸铜;
(3)根据CuSO4溶液与足量Ba(OH)2溶液的反应来写出离子方程式.
| ||
(2)物质中均含氧元素,Cu与浓硫酸、CuO与硫酸、氢氧化铜与硫酸、氯化钡与硫酸均可生成硫酸铜;
(3)根据CuSO4溶液与足量Ba(OH)2溶液的反应来写出离子方程式.
解答:
解:(1)A物质可以导致酸雨的形成,则A是二氧化硫,应该属于酸性氧化物,A物质可以使酸性KMnO4溶液褪色,此反应中SO2 失去电子,氧化剂是KMnO4,
故答案为:d;SO2;
(2)CuSO4溶液、CuSO4?5H2O、Cu(OH)2、液态O2物质中均含氧元素,Cu与浓硫酸、CuO与硫酸、氢氧化铜与硫酸、碳酸铜与硫酸均可生成硫酸铜,
故答案为:均含有氧元素;abcd;
(3)CuSO4溶液与足量Ba(OH)2的化学方程式:CuSO4+Ba(OH)2=BaSO4↓+Cu(OH)2↓,在书写离子方程式的时候,能拆的物质有强酸、强碱和可溶性盐,故
离子方程式为:Cu2++SO42-+Ba2++2OH-=BaSO4↓+Cu(OH)2↓,故答案为:Cu2++SO42-+Ba2++2OH-=BaSO4↓+Cu(OH)2↓
故答案为:d;SO2;
(2)CuSO4溶液、CuSO4?5H2O、Cu(OH)2、液态O2物质中均含氧元素,Cu与浓硫酸、CuO与硫酸、氢氧化铜与硫酸、碳酸铜与硫酸均可生成硫酸铜,
故答案为:均含有氧元素;abcd;
(3)CuSO4溶液与足量Ba(OH)2的化学方程式:CuSO4+Ba(OH)2=BaSO4↓+Cu(OH)2↓,在书写离子方程式的时候,能拆的物质有强酸、强碱和可溶性盐,故
离子方程式为:Cu2++SO42-+Ba2++2OH-=BaSO4↓+Cu(OH)2↓,故答案为:Cu2++SO42-+Ba2++2OH-=BaSO4↓+Cu(OH)2↓
点评:本题考查了物质的分类方法和二氧化硫的性质以及离子方程式的书写,难度不大.

练习册系列答案
相关题目
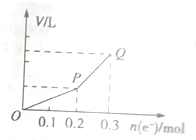 用惰性电极电解硫酸铜溶液,整个过程转移电子的物质的量与产生气体总体积的关系如图所示(气体体积均在相同状况下测定).欲使溶液恢复到起始状态,可向溶液中加入( )
用惰性电极电解硫酸铜溶液,整个过程转移电子的物质的量与产生气体总体积的关系如图所示(气体体积均在相同状况下测定).欲使溶液恢复到起始状态,可向溶液中加入( )| A、0.1molCuO |
| B、0.1molCuCO3 |
| C、0.1molCu(OH)2 |
| D、0.05molCu2(OH)2CO3 |
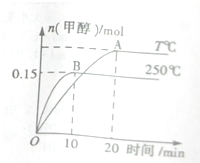 将1molCO和2molH2充入一容积为1L的密闭容器中,分别在250℃、T℃下发生反应:CO(g)+2H2(g)?CH3OH(g)△H=a KJ?mol-1,如图所示,下列分析中正确的是( )
将1molCO和2molH2充入一容积为1L的密闭容器中,分别在250℃、T℃下发生反应:CO(g)+2H2(g)?CH3OH(g)△H=a KJ?mol-1,如图所示,下列分析中正确的是( )| A、250℃时,0~10minH2反应速率为0.015mol?(L?Min)-1 |
| B、平衡时CO的转化率:T℃时小于250℃时 |
| C、a>0 |
| D、平衡常数K:T℃时大于250℃ |
反应C (s)+CO2(g)?2CO(g)在恒容容器、一定温度下达到平衡,再充入CO2,达到
新的平衡时(温度不变),与原平衡比,以下正确的是( )
新的平衡时(温度不变),与原平衡比,以下正确的是( )
| A、平衡向正反应方向移动 |
| B、混合气体的平均摩尔质量增大 |
| C、CO2的转化率增大 |
| D、逆反应速率减小 |
下列体系加压后,对化学反应速率没有影响的是( )
| A、2SO2+O2?2SO3 |
| B、CO+H2O(g)?CO2+H2 |
| C、CO2+H2O?H2CO3 |
| D、H++OH-?H2O |
下列反应属于氧化还原反应的是( )
| A、CaCO3+2HCl=CaCl2+H2O+CO2↑ |
| B、SO2+H2O=H2SO3 |
| C、Cl2+2NaOH=NaCl+NaClO+H2O |
| D、NaBr+AgNO3=AgBr↓+NaNO3 |