题目内容
10.欲除去下列物质中的杂质(括号内为杂质),所选用的方法不妥当的是( )| A. | 乙酸乙酯(乙酸):加入乙醇和浓硫酸,然后加热 | |
| B. | 碳酸钠固体(碳酸氢钠):加热至恒重 | |
| C. | FeCl2溶液(FeCl3、CuCl2):加入过量Fe粉充分搅拌,然后过滤 | |
| D. | 乙醇(水):加入新制的生石灰,然后蒸馏 |
分析 A.乙酸与乙醇的反应为可逆反应;
B.碳酸氢钠不稳定,解热易分解;
C.铁可与FeCl3、CuCl2反应生成FeCl2;
D.生石灰可与水反应,蒸馏得到乙醇.
解答 解:A.乙酸与乙醇的反应为可逆反应,不能得到纯净的乙酸乙酯,可用饱和碳酸钠溶液除杂,故A错误;
B.碳酸氢钠不稳定,解热易分解,可用加热的方法除杂,故B正确;
C.铁可与FeCl3、CuCl2反应生成FeCl2,可除去杂质,故C正确
D.生石灰可与水反应,蒸馏得到乙醇,可除去杂质,故D正确.
故选A.
点评 本题考查混合物分离提纯,为高频考点,把握物质的性质、性质差异及混合物分离提纯方法为解答的关键,侧重分析与应用能力的考查,注意有机物的性质应用,题目难度不大.

练习册系列答案
相关题目
20.将2g甲醛溶于3g醋酸中,再加入4gα-羟基丙酸[CH3CH(OH)COOH],混合均匀后在足量氧气中完全燃烧,生成水的质量为( )
| A. | 5.4g | B. | 6.3g | C. | 7.2g | D. | 9.0g |
18.具有真正意义上的元素周期表是由哪位化学家发现的是( )
| A. | 门捷列夫(俄国) | B. | 依马林(俄国) | ||
| C. | 别洛索夫(俄国) | D. | 马尔柯夫尼可夫(俄国) |
2.下列叙述中正确的是( )
| A. | 离子化合物中一定含有金属元素 | |
| B. | 分子晶体、原子晶体中一定含有共价键,离子晶体一定含有离子键 | |
| C. | 气态氢化物的稳定性:NH3>PH3>AsH3 | |
| D. | 正四面体结构的分子中的键角一定是109°28′ |
19.下列各组物质反应后,再滴入KSCN溶液,显红色的是( )
| A. | 向CuCl2溶液中加入铁粉 | |
| B. | 向FeO粉末中加入稀硫酸 | |
| C. | 单质Fe与过量稀盐酸反应后的溶液中再加入少量氯水 | |
| D. | Fe(OH)3与过量稀盐酸反应后的溶液中再加入过量铁粉 |
20.下列离子方程式,正确的是( )
| A. | 氯化铝溶液与过量氨水 Al3++3NH3•H2O=Al(OH)3↓+3NH4+ | |
| B. | 明矾净水原理:Al3++3H2O→Al(OH)3↓+3H+ | |
| C. | 将足量氯气通入溴化亚铁溶液:2Fe2++Cl2→2Fe3++2Cl- | |
| D. | 偏铝酸钠溶液与过量盐酸AlO2-+H++H2O→Al(OH)3↓ |
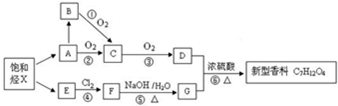
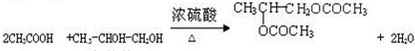 .
.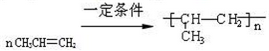 .
.