题目内容
15.实验测得某化合物A只由C、H、O三种元素组成,而且1molA完全燃烧需消耗4molO2.已知A不与金属钠发生反应,A可被催化氧化生成B,且0.37gB可与25mL0.20mol/L的NaOH溶液刚好完全反应.试通过计算确定化合物A的分子式和B可能的结构简式.分析 A不与金属钠发生反应,说明不含羟基,A可被催化氧化生成B,且B可与NaOH溶液反应,可说明A为醛,B为酸,n(NaOH)=0.025L×0.20mol/L=0.005mol,如B为一元酸,则B的物质的量为0.005mol,相对分子质量为$\frac{0.37}{0.005}$=74,具有R-COOH结构,可知M(R)=74-45=29,则R应为C2H5-,则A为C2H5CHO,1molA完全燃烧需消耗氧气的物质的量为(3+$\frac{6}{4}$-$\frac{1}{2}$)mol=4mol,符合题目要求,以此解答该题.
解答 解:A不与金属钠发生反应,说明不含羟基,A可被催化氧化生成B,且B可与NaOH溶液反应,可说明A为醛,B为酸,n(NaOH)=0.025L×0.20mol/L=0.005mol,如B为一元酸,则B的物质的量为0.005mol,相对分子质量为$\frac{0.37}{0.005}$=74,具有R-COOH结构,可知M(R)=74-45=29,则R应为C2H5-,则A为C2H5CHO,1molA完全燃烧需消耗氧气的物质的量为(3+$\frac{6}{4}$-$\frac{1}{2}$)mol=4mol,符合要求,则A的分子式为C3H6O,B可能的结构简式为CH3CH2COOH,
答:化合物A的分子式为C3H6O,B可能的结构简式为CH3CH2COOH.
点评 本题考查有机的推断,为高频考点,侧重考查学生分析判断能力,明确有机物中官能团及其性质关系,题目难度不大.

练习册系列答案
相关题目
5.某无色混合气体,将其依次通过浓H2SO4和Na2O2,若气体体积不断减小,最后颜色变深,则混合气体的成分可能是( )
| A. | N2、H2O、NO | B. | NH3、CO2、NO | C. | NH3、O2、NO | D. | H2O、NO2、CO2 |
3.在下列反应中,浓硫酸既表现强氧化性,又表现酸性的是( )
| A. | NaCl+H2SO4(浓) | B. | Cu+H2SO4(浓) | C. | C+H2SO4(浓) | D. | CuO+H2SO4(浓) |
10.欲除去下列物质中的杂质(括号内为杂质),所选用的方法不妥当的是( )
| A. | 乙酸乙酯(乙酸):加入乙醇和浓硫酸,然后加热 | |
| B. | 碳酸钠固体(碳酸氢钠):加热至恒重 | |
| C. | FeCl2溶液(FeCl3、CuCl2):加入过量Fe粉充分搅拌,然后过滤 | |
| D. | 乙醇(水):加入新制的生石灰,然后蒸馏 |
7. 25℃时,三种酸的电离常数为:
25℃时,三种酸的电离常数为:
请回答下列问题:
(1)物质的量浓度为0.1mol/L的下列物质:a.Na2CO3、b.NaClO、c.CH3COONa、d.NaHCO3;pH由大到小的顺序是:abdc(填编号)
(2)常温下0.1mol/L的CH3COOH在水中约有1%发生电离,其溶液的pH=3,将该溶液加蒸馏水稀释,在稀释过程中,下列表达式的数据变大的是:BD.
A.c(H+) B.c(H+)/c(CH3COOH)
C.c(H+)•c(OH-) D.c(OH-)/c(H+)
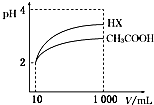
(3)体积为10mL pH=2的醋酸溶液与一元酸HX分别加蒸馏水稀释至1 000mL,稀释过程pH变化如图;则HX的电离平衡常数大于(填“大于”、“等于”或“小于”)醋酸的电离平衡常数;稀释后,HX溶液中水电离出来的c(H+)大于醋酸溶液水电离出来的c(H+)(填“大于”、“等于”或“小于”).
(4)25℃时,CH3COOH与CH3COONa的混合溶液,若测得混合液pH=6,则溶液中:c(CH3COO-)-c(Na+)=9.9×10-7mol/L(填准确数值).
 25℃时,三种酸的电离常数为:
25℃时,三种酸的电离常数为:| 化学式 | CH3COOH | H2CO3 | HClO |
| 电离平衡常数K | 1.8×10-5 | K1=4.3×10-7 K2=5.6×10-11 | 3.0×10-8 |
(1)物质的量浓度为0.1mol/L的下列物质:a.Na2CO3、b.NaClO、c.CH3COONa、d.NaHCO3;pH由大到小的顺序是:abdc(填编号)
(2)常温下0.1mol/L的CH3COOH在水中约有1%发生电离,其溶液的pH=3,将该溶液加蒸馏水稀释,在稀释过程中,下列表达式的数据变大的是:BD.
A.c(H+) B.c(H+)/c(CH3COOH)
C.c(H+)•c(OH-) D.c(OH-)/c(H+)
(3)体积为10mL pH=2的醋酸溶液与一元酸HX分别加蒸馏水稀释至1 000mL,稀释过程pH变化如图;则HX的电离平衡常数大于(填“大于”、“等于”或“小于”)醋酸的电离平衡常数;稀释后,HX溶液中水电离出来的c(H+)大于醋酸溶液水电离出来的c(H+)(填“大于”、“等于”或“小于”).
(4)25℃时,CH3COOH与CH3COONa的混合溶液,若测得混合液pH=6,则溶液中:c(CH3COO-)-c(Na+)=9.9×10-7mol/L(填准确数值).
5.在强酸性溶液中能大量共存的离子组是( )
| A. | K+、Na+、NO3-、CO32- | B. | Ba2+、Na+、Cl-、SO42- | ||
| C. | K+、Na+、Cl-、NO3- | D. | Na+、Mg2+、OH-、NO3- |

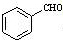
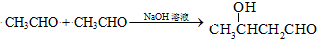 (甘氨酸)
(甘氨酸)
 ;
; $\stackrel{催化剂}{→}$
$\stackrel{催化剂}{→}$ .
.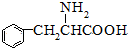 至少需要a步化学反应.
至少需要a步化学反应.
 CH3COOCH2CH3+H2O
CH3COOCH2CH3+H2O