题目内容
只用一种试剂可区别Na2SO4、MgCl2、NH4Cl、FeCl3四种溶液,这种试剂是( )
| A、NaOH |
| B、H2SO4 |
| C、BaCl2 |
| D、AgNO3 |
考点:物质的检验和鉴别的基本方法选择及应用
专题:物质检验鉴别题
分析:Na2SO4、MgCl2、NH4Cl、FeCl3四种溶液分别与NaOH混合的现象为:无现象、白色沉淀、刺激性气体、红褐色沉淀,以此来解答.
解答:
解:A.Na2SO4、MgCl2、NH4Cl、FeCl3四种溶液分别与NaOH混合的现象为:无现象、白色沉淀、刺激性气体、红褐色沉淀,现象不同可鉴别,故A选;
B.均不与硫酸反应,现象相同,不能鉴别,故B不选;
C.MgCl2、NH4Cl、FeCl3均不与BaCl2反应,现象相同,不能鉴别,故C不选;
D.均与硝酸银反应生成白色沉淀,现象相同,不能鉴别,故D不选;
故选A.
B.均不与硫酸反应,现象相同,不能鉴别,故B不选;
C.MgCl2、NH4Cl、FeCl3均不与BaCl2反应,现象相同,不能鉴别,故C不选;
D.均与硝酸银反应生成白色沉淀,现象相同,不能鉴别,故D不选;
故选A.
点评:本题考查物质的检验及鉴别,为高频考点,明确物质的性质是解答此类习题的关键,注意现象不同即可鉴别,若现象相同不能鉴别,题目难度不大.

练习册系列答案
相关题目
用标准盐酸滴定氢氧化钠溶液测碱液浓度时,下列操作导致所测的碱液浓度一定偏低的是( )
| A、滴定后酸式滴定管尖嘴处悬有一滴液体 |
| B、酸式滴定管洗净后,没有用标准盐酸润洗,直接装标准盐酸滴定碱液 |
| C、滴定前,酸式滴定管有气泡,滴定后消失 |
| D、记录所用盐酸体积时,先仰视读数,终点时俯视 |
下列分离或提纯物质的方法正确的是( )
| A、用渗析的方法精制Fe(OH)3胶体 |
| B、用过滤的方法除去NaCl溶液中含有的少量淀粉胶体 |
| C、用溶解、过滤的方法提纯含有少量BaSO4的BaCO3 |
| D、用加热蒸发结晶的方法从AlCl3溶液得到AlCl3 |
700℃时,向容积为2L的密闭容器中充入一定量的CO和H2O,发生反应:CO(g)+H2O(g)?CO2+H2(g) 反应过程中测定的部分数据见表(表中t1>t2):下列说法不正确的是( )
| 反应时间/min | n(CO)/mol | H2O/mol |
| 0 | 1.20 | 0.60 |
| t1 | 0.80 | |
| t2 | 0.20 |
| A、保持其他条件不变,向平衡体系中再通入0.20molH2O,与原平衡相比,达到新平衡时CO转化率增大,H2O的体积分数增大 | ||
| B、保持其他条件不变,起始时向容器中充入0.60molCO和1.20 molH2O,到达平衡时,n(CO2)=0.40 mol | ||
C、反应在t1min内的平均速率为v(H2)=
| ||
| D、温度升至800℃,上述反应平衡常数为0.64,则正反应为放热反应 |
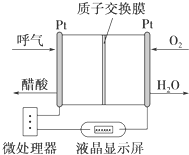 如图所示是一种酸性燃料电池酒精检测仪,具有自动吹气流量侦测与控制的功能,非常适合进行现场酒精检测.下列说法不正确的是( )
如图所示是一种酸性燃料电池酒精检测仪,具有自动吹气流量侦测与控制的功能,非常适合进行现场酒精检测.下列说法不正确的是( )| A、电流由O2所在的铂电极经外电路流向另一电极 |
| B、O2所在的铂电极处发生还原反应 |
| C、该电池的负极反应式为:CH3CH2OH+3H2O-12e-═2CO2↑+12H+ |
| D、微处理器通过检测电流大小而计算出被测气体中酒精的含量 |