题目内容
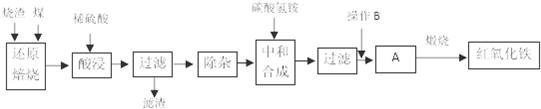
硫铁矿烧渣是硫铁矿生产硫酸过程中产生的工业废渣(主要含Fe2O3及少量SiO2、A12O3等杂质).用该烧渣制取药用辅料-红氧化铁的工艺流程如下:
(1)在“还原焙烧”中产生的有毒气体可能有 .
(2)“酸浸”时间一般不超过20min,若在空气中酸浸时间过长,溶液中Fe2+含量将下降,其原因是 (用离子方程式表示).
(3)“中和合成”的目的是将溶液中Fe2+转变为碳酸亚铁沉淀,则操作B是 .
(4)煅烧A的反应方程式是 .
(5)ag烧渣经过上述工艺可得红氧化铁bg.药典标准规定,制得的红氧化铁中含氧化铁不得少于98.0%,则所选用的烧渣中铁的质量分数应不低于 (用含a、b的表达式表示).

(1)在“还原焙烧”中产生的有毒气体可能有
(2)“酸浸”时间一般不超过20min,若在空气中酸浸时间过长,溶液中Fe2+含量将下降,其原因是
(3)“中和合成”的目的是将溶液中Fe2+转变为碳酸亚铁沉淀,则操作B是
(4)煅烧A的反应方程式是
(5)ag烧渣经过上述工艺可得红氧化铁bg.药典标准规定,制得的红氧化铁中含氧化铁不得少于98.0%,则所选用的烧渣中铁的质量分数应不低于
考点:物质分离和提纯的方法和基本操作综合应用
专题:实验设计题
分析:工业废渣主要含Fe2O3及少量SiO2、A12O3、CaO、MgO等杂质,加煤燃烧可生成CO、SO2等有毒气体,加硫酸后只有二氧化硅不反应,酸浸时间过长,溶液中Fe2+含量将下降,被氧化生成Fe3+,过滤除去二氧化硅,然后除杂时结合生成沉淀的pH可知,pH大于4.77,小于7.11时Fe3+和Al3+完全转化为沉淀,而亚铁离子没有转化为沉淀,“中和合成”的目的是将溶液中Fe2+转变为碳酸亚铁沉淀,过滤得到A为碳酸亚铁,需要洗涤、干燥,然后加热得到氧化铁,以此来解答.
解答:
解:工业废渣主要含Fe2O3及少量SiO2、A12O3、CaO、MgO等杂质,加煤燃烧可生成CO、SO2等有毒气体,加硫酸后只有二氧化硅不反应,酸浸时间过长,溶液中Fe2+含量将下降,被氧化生成Fe3+,过滤除去二氧化硅,然后除杂时结合生成沉淀的pH可知,pH大于4.77,小于7.11时Fe3+和Al3+完全转化为沉淀,而亚铁离子没有转化为沉淀,“中和合成”的目的是将溶液中Fe2+转变为碳酸亚铁沉淀,过滤得到A为碳酸亚铁,需要洗涤、干燥,然后加热得到氧化铁,
(1)由上述分析可知,“还原焙烧”中产生的有毒气体可能有CO、SO2等,故答案为:CO、SO2等;
(2)在空气中酸浸时间过长,溶液中Fe2+含量将下降,其原因是4Fe2++O2+4H+=4Fe3++2H2O,故答案为:4Fe2++O2+4H+=4Fe3++2H2O;
(3)A为碳酸亚铁,需要洗涤、干燥,然后加热得到氧化铁,故答案为:洗涤、干燥;
(4)煅烧A(FeCO3)生成氧化铁,反应方程式为:4FeCO3+O2
2Fe2O3+4CO2,故答案为:4FeCO3+O2
2Fe2O3+4CO2;
(5)制得的红氧化铁中含氧化铁不得少于98.0%,制取的红氧化铁bg中含有的铁的物质的量应该大于:
×2=
mol,则所选用的烧渣中铁的质量分数应不低于:
=
,故答案为:
.
(1)由上述分析可知,“还原焙烧”中产生的有毒气体可能有CO、SO2等,故答案为:CO、SO2等;
(2)在空气中酸浸时间过长,溶液中Fe2+含量将下降,其原因是4Fe2++O2+4H+=4Fe3++2H2O,故答案为:4Fe2++O2+4H+=4Fe3++2H2O;
(3)A为碳酸亚铁,需要洗涤、干燥,然后加热得到氧化铁,故答案为:洗涤、干燥;
(4)煅烧A(FeCO3)生成氧化铁,反应方程式为:4FeCO3+O2
| ||
| ||
(5)制得的红氧化铁中含氧化铁不得少于98.0%,制取的红氧化铁bg中含有的铁的物质的量应该大于:
| bg×98% |
| 160g/mol |
| b×98% |
| 80 |
| ||
| ag |
| 7b×98% |
| 10a |
| 7b×98% |
| 10a |
点评:本题考查制备实验方案的设计,为高频考点,把握制备原理及实验流程中的反应、物质的性质等为解答的关键,侧重分析与实验、计算能力的综合考查,题目难度不大.

练习册系列答案
相关题目
本地的自来水是采用氯气消毒的,为了检验Cl-的存在,最好选用下列物质中( )
| A、石蕊溶液 |
| B、四氯化碳 |
| C、氢氧化钠溶液 |
| D、硝酸酸化的硝酸银溶液 |
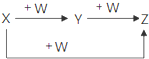 X、Y、Z、W有如图所示的转化关系,则X、W可能是( )
X、Y、Z、W有如图所示的转化关系,则X、W可能是( )①AlCl3、NaOH ②C、O2 ③Cl2、Fe ④S、O2.
| A、①②③ | B、①② |
| C、③④ | D、①②③④ |
只用一种试剂可区别Na2SO4、MgCl2、NH4Cl、FeCl3四种溶液,这种试剂是( )
| A、NaOH |
| B、H2SO4 |
| C、BaCl2 |
| D、AgNO3 |
 某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:
某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下: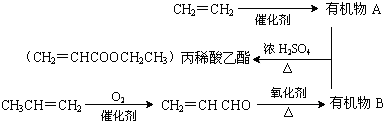
 )对花香和果香的香韵具有提升作用,故常用于化妆品和食品工业.乙酸苯甲酯的合成路线如图:
)对花香和果香的香韵具有提升作用,故常用于化妆品和食品工业.乙酸苯甲酯的合成路线如图: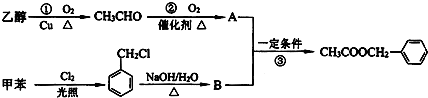
 )互为同系物的是
)互为同系物的是 B.
B.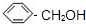 C.
C.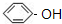 D.
D.
 C.2CH3CHO+H2
C.2CH3CHO+H2