题目内容
2.甲、乙、丙、丁分别是硫酸铝、硫酸铁、氢氧化钠、氯化钡等四种物质中的一种,若将丁溶液滴入乙溶液中,发现有白色沉淀生成,继续滴加则沉淀消失.丁溶液滴入甲溶液中,无明显现象发生.据此可推断丙物质是( )| A. | Fe2(SO4)3 | B. | NaOH | C. | Al2(SO4)3 | D. | BaCl2 |
分析 若将丁溶液滴入乙溶液中,发现有白色沉淀生成,继续滴加则沉淀消失,应为NaOH和Al2(SO4)3的反应,则丁为NaOH,乙为Al2(SO4)3,丁溶液滴入甲溶液中,无明显现象发生,只有BaCl2与NaOH不反应,则甲为BaCl2,以此来解答.
解答 解:因氢氧化铝具有两性,则由丁溶液滴入乙溶液中,发现有白色沉淀生成,继续滴加则沉淀消失,应为NaOH和Al2(SO4)3的反应,则丁为NaOH,乙为Al2(SO4)3;丁溶液滴入甲溶液中,无明显现象发生,只有BaCl2与NaOH不反应,则甲为BaCl2,可知剩余一种物质丙为Fe2(SO4)3,
故选A.
点评 本题考查无机物的推断,为高频考点,把握根据物质反应的现象进行推断为解答的关键,注意氢氧化铝的两性为突破口,学习中注意常见元素化合物知识的积累,题目难度不大.

练习册系列答案
相关题目
12.有机物X(C4H6O5)广泛存在于许多水果内,尤以苹果、葡萄、西瓜、山楂内为多,该化合物具有如下性质:
(1)1molX与足量的金属钠反应产生1.5mol气体
(2)X与醇或羧酸在浓H2SO4和加热的条件下均生成有香味的产物
(3)X在一定程度下的分子内脱水产物(不是环状化合物)可和溴水发生加成反应根据上述信息
对X的结构判断正确的是( )
(1)1molX与足量的金属钠反应产生1.5mol气体
(2)X与醇或羧酸在浓H2SO4和加热的条件下均生成有香味的产物
(3)X在一定程度下的分子内脱水产物(不是环状化合物)可和溴水发生加成反应根据上述信息
对X的结构判断正确的是( )
| A. | X中可能有两个羧基和一个羟基 | |
| B. | X中可能有三个羟基和一个 一COOR官能团 | |
| C. | X中肯定有碳碳双键 | |
| D. | X中可能有三个羧基 |
13.Ⅰ:工业制硫酸时,利用接触氧化反应将SO 2转化为SO3是一个关键步骤.
(1)某温度下,2SO2(g)+O 2(g)?2SO3(g)△H=-197kJ/mol.开始时在10L的密闭容器中加入8.0mol SO2(g)和20.0mol O 2(g),当反应达到平衡时共放出394kJ的热量,该温度下的平衡常数K=0.56(保留两位有效数字),若升高温度时,K将减小(填“增大、减小或不变”).
(2)若体积不变的条件下,下列措施中有利于提高SO2的转化率条件是AC(填字母).
A.通入氧气 B.移出氧气 C.增大压强 D.减小压强 E.加入催化剂
(3)在硫酸工业生产过程中,有反应2SO2(g)+O2(g)?2SO3(g)(正反应为放热反应),根据下表提供的不同条件下SO2的转化率(%)的数据,试选择该反应的适宜条件(以V2O5作催化剂)温度450℃;压强1×105Pa.
(4)能判断该反应达到平衡状态的依据是ACF.
A.容器的压强不变 B.混合气体的密度不变
C.混合气体中SO 3的浓度不变 D.C(SO 2)=C(SO 3)
E.v 正(SO 2)=v 正(SO 3) F.v 正(SO 3)=2v 逆(O 2)
Ⅱ:研究化学反应原理对于生产生活是很有意义的.
(1)在0.10mol•L-1硫酸铜溶液中加入氢氧化钠稀溶液充分搅拌,有浅蓝色氢氧化铜沉淀生成,当溶液的pH=8时,c(Cu2+)=2.2×10-8mol•L-1(Ksp[Cu(OH)2]=2.2×10-20).
(2)若在0.1mol•L-1硫酸铜溶液中通入H2S气体,使Cu2+完全沉淀为CuS,此时溶液中的H+浓度是0.2mol•L-1.
(1)某温度下,2SO2(g)+O 2(g)?2SO3(g)△H=-197kJ/mol.开始时在10L的密闭容器中加入8.0mol SO2(g)和20.0mol O 2(g),当反应达到平衡时共放出394kJ的热量,该温度下的平衡常数K=0.56(保留两位有效数字),若升高温度时,K将减小(填“增大、减小或不变”).
(2)若体积不变的条件下,下列措施中有利于提高SO2的转化率条件是AC(填字母).
A.通入氧气 B.移出氧气 C.增大压强 D.减小压强 E.加入催化剂
(3)在硫酸工业生产过程中,有反应2SO2(g)+O2(g)?2SO3(g)(正反应为放热反应),根据下表提供的不同条件下SO2的转化率(%)的数据,试选择该反应的适宜条件(以V2O5作催化剂)温度450℃;压强1×105Pa.
| 1×105Pa | 5×105Pa | 10×105Pa | 50×105Pa | 100×105Pa | |
| 450℃ | 97.5 | 98.9 | 99.2 | 99.6 | 99.7 |
| 500℃ | 85.6 | 92.9 | 94.9 | 97.7 | 98.3 |
A.容器的压强不变 B.混合气体的密度不变
C.混合气体中SO 3的浓度不变 D.C(SO 2)=C(SO 3)
E.v 正(SO 2)=v 正(SO 3) F.v 正(SO 3)=2v 逆(O 2)
Ⅱ:研究化学反应原理对于生产生活是很有意义的.
(1)在0.10mol•L-1硫酸铜溶液中加入氢氧化钠稀溶液充分搅拌,有浅蓝色氢氧化铜沉淀生成,当溶液的pH=8时,c(Cu2+)=2.2×10-8mol•L-1(Ksp[Cu(OH)2]=2.2×10-20).
(2)若在0.1mol•L-1硫酸铜溶液中通入H2S气体,使Cu2+完全沉淀为CuS,此时溶液中的H+浓度是0.2mol•L-1.
10.下图所示的实验操作中,正确的是( )
| A. |  取用药品 | B. | 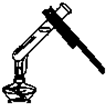 给试管加热 | ||
| C. | 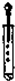 滴加液体 | D. | 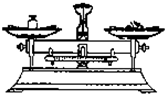 称量10.05g固体 |
17.下列反应的离子方程式书写正确的是( )
| A. | 氯化铝与过量氨水:Al3++4OH-═AlO2-+H2O | |
| B. | 钠和冷水反应:Na+2H2O═Na++2OH-?+H2↑ | |
| C. | 氯气与水反应Cl2+H2O?Cl-+H++HClO | |
| D. | 碳酸钙与盐酸反应:CO32-+2H+═H2O+CO2↑ |
7.用惰性电极电解下列溶液,一段时间后,再加入一定质量的另一物质(括号内),溶液一定不能与原来溶液一样的是( )
| A. | CuCl2(CuCl2) | B. | AgNO3(Ag2O) | C. | NaCl(NaCl) | D. | CuSO4[Cu(OH)2] |
14.设NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 25℃时,1L pH=ll的CH3COONa溶液中水电离出的OH-的数目为0.001NA | |
| B. | 28g乙烯和丙烯的混合气体含有的原子个数为3NA | |
| C. | 1 mol/L-l NaHCO3溶液中含有HCO3-数目小于NA | |
| D. | 6.8g液态KHSO4中含有0.1NA个阳离子 |
11.下列离子方程式书写正确的是( )
| A. | 碳酸钙与盐酸反应 CO32-+2H+═CO2↑+H2O | |
| B. | 往CuCl2溶液中加入钠 2Na+Cu2+═2Na++Cu | |
| C. | 铁与稀硫酸反应 Fe+2H+═Fe2++H2↑ | |
| D. | 稀硫酸与氢氧化钡溶液反应 H++SO42-+Ba2++OH-═H2O+BaSO4↓ |
12.NaNO2是一种食品添加剂,能致癌.酸性KMnO4溶液与NaNO2反应的离子方程式是:MnO4-+NO2-+□→Mn2++NO3-+H2O (未配平),下列叙述中正确的是( )
| A. | 该反应中NO2-被还原 | |
| B. | 生成1mol NaNO3需消耗0.4mol KMnO4 | |
| C. | 反应过程中溶液的pH减小 | |
| D. | □中的粒子是OH- |