题目内容
10.下图所示的实验操作中,正确的是( )| A. |  取用药品 | B. | 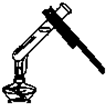 给试管加热 | ||
| C. | 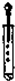 滴加液体 | D. | 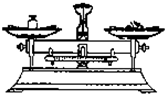 称量10.05g固体 |
分析 A.取用药品,不能用手,有些药品有毒或有腐蚀性;并且会污染药品;
B.给试管加热:先预热再集中加热,注意试管的倾斜角度;
C.使用胶头滴管滴加少量液体的操作,注意胶头滴管的位置是否伸入到试管内或接触试管内壁.应垂直悬空在试管口上方滴加液体,防止污染胶头滴管;
D.称量物质时,物质不能直接放在托盘上,会污染托盘;且应“左物右码”.
解答 解:A.取用药品,不能用手,有些药品有毒或有腐蚀性,应用药匙或镊子,图中操作错误,故A错误;
B.给液体加热时,①先预热再集中加热,;②试管与桌面成约45°角,图中操作正确,故B正确;
C.胶头滴管伸入试管内或接触试管,会造成药品的污染,图中操作错误,故C错误;
D.物质不能直接放在托盘上,会污染托盘,并且,物质和砝码的物质放反;称量10.05g固体,精确度达不到,故D错误.
故选B.
点评 本题考查较为综合,涉及基础实验操作,侧重于学生的分析能力和实验能力的考查,为高频考点,注意把握实验的方法、步骤和使用的仪器,注重相关基础知识的积累,难度不大.

练习册系列答案
 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
相关题目
1.在实验室里做钠跟水反应的实验时,用到的仪器是( )
a.试管夹 b.镊子 c.小刀 d.冷凝管 e.滤纸 f.研钵 g.烧杯h.坩埚i.石棉网 j.玻璃片 k.药匙 l.燃烧匙.
a.试管夹 b.镊子 c.小刀 d.冷凝管 e.滤纸 f.研钵 g.烧杯h.坩埚i.石棉网 j.玻璃片 k.药匙 l.燃烧匙.
| A. | abdi | B. | cefk | C. | fghl | D. | bcegj |
5.用已知浓度的盐酸滴定未知浓度的NaOH溶液,选用酚酞作指示剂,下列操作会导致测定结果偏低的是( )
| A. | 酸式滴定管未润洗就装标准液滴定 | |
| B. | 锥形瓶未用待测液润洗 | |
| C. | 滴定前酸式滴定管尖嘴处有气泡未排除,滴定后气泡消失 | |
| D. | 读取标准液读数时,滴前仰视,滴定到终点后俯视 |
2.甲、乙、丙、丁分别是硫酸铝、硫酸铁、氢氧化钠、氯化钡等四种物质中的一种,若将丁溶液滴入乙溶液中,发现有白色沉淀生成,继续滴加则沉淀消失.丁溶液滴入甲溶液中,无明显现象发生.据此可推断丙物质是( )
| A. | Fe2(SO4)3 | B. | NaOH | C. | Al2(SO4)3 | D. | BaCl2 |
19.X、Y、Z、T、V为5种短周期元素,X、Y、Z在周期表中位置如图所示.这3种元素 原子序数之和是41,X和T在不同条件下反应,可以生成T2X(白色固体)和T2X2(淡黄 色固体)两种化合物.V单质在Z单质中燃烧产生苍白色火焰,产物溶于水能使紫色石蕊溶液变 红,则:
(1)5种元素的元素符号分别是XO,YS,ZCl,TNa,VH.
(2)Y的原子结构示意图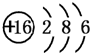 .
.
(3)T与X形成化合物T2X与T2X2的化学方程式分别为4Na+O2=2Na2O,2Na+O2=Na2O2.
| X | |
| Y | Z |
(2)Y的原子结构示意图
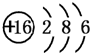 .
.(3)T与X形成化合物T2X与T2X2的化学方程式分别为4Na+O2=2Na2O,2Na+O2=Na2O2.