题目内容
3.下列有关溶液组成的描述合理的是( )| A. | 漂白粉的水溶液可能大量存在Fe2+、Cl-、Ca2+、Na+ | |
| B. | 滴加石蕊呈红色的溶液可能大量存在K+、NH4+、Cl-、S2- | |
| C. | 与Al反应能放出H2的溶液中可能大量存在:Fe2+、K+、NO3-、SO42- | |
| D. | 弱碱性溶液中可能大量存在Na+、K+、Cl-、HCO3- |
分析 A.漂白粉具有强氧化性;
B.滴加石蕊呈红色的溶液,显酸性;
C.与Al反应能放出H2的溶液,为非氧化性酸或强碱溶液;
D.该组离子之间不反应.
解答 解:A.漂白粉具有强氧化性,与Fe2+发生氧化还原反应不能共存,故A错误;
B.滴加石蕊呈红色的溶液,显酸性,不能大量存在S2-,故B错误;
C.与Al反应能放出H2的溶液,为非氧化性酸或强碱溶液,碱性溶液中不能大量存在Fe2+,酸溶液中Fe2+、H+、NO3-发生氧化还原反应,故C错误;
D.该组离子之间不反应,可大量共存,故D正确;
故选D.
点评 本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重分析与应用能力的考查,注意复分解反应、氧化还原反应的判断,题目难度不大.

练习册系列答案
相关题目
18.如图1为甲烷和O2构成的燃料电池示意图,电解质为KOH溶液,图2为电解AlCl3溶液的装置,电极材料均为石墨.用该装置进行实验,反应开始后观察到x电极附近出现白色沉淀.下列说法正确的是( )

| A. | A处通入的气体为CH4,电极反应式为:CH4+10OH--8e-═CO32-+7H2O | |
| B. | 图2中电解AlCl3溶液的总反应为:2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$Cl2↑+H2↑+2OH- | |
| C. | 图1中电解质溶液的pH增大 | |
| D. | 电解池中Cl-向x极移动 |
19.下列关于有机物的说法正确的是( )
| A. | 甲烷与氯气发生取代反应,只能生成一氯甲烷 | |
| B. | 乙醇和乙酸都可以与钠反应生成氢气 | |
| C. | 苯和乙烯均能与溴水发生加成反应使溴水褪色 | |
| D. | 甲醛易溶于水,其水溶液具有杀菌消毒作用,可用于浸泡海鲜食品 |
18.下列叙述正确的是( )
①氧化铝是一种比较好的耐火材料,可用来制造耐火坩埚
②氧化铁常用作红色油漆和涂料
③碳酸氢钠俗名小苏打,可用于制作发酵粉
④过氧化钠比氧化钠稳定,是碱性氧化物
⑤焰色反应体现的是元素的性质.
①氧化铝是一种比较好的耐火材料,可用来制造耐火坩埚
②氧化铁常用作红色油漆和涂料
③碳酸氢钠俗名小苏打,可用于制作发酵粉
④过氧化钠比氧化钠稳定,是碱性氧化物
⑤焰色反应体现的是元素的性质.
| A. | ①②③⑤ | B. | ②③④⑤ | C. | ①③④⑤ | D. | ①②③④ |
15.根据下列实验操作和现象得出的结论正确的是( )
| 选项 | 实验操作 | 现象 | 结论 |
| A | 将某溶液与稀盐酸反应产生的气体通入澄清石灰水 | 石灰水变浑浊 | 该溶液中一定含有CO32- |
| B | 将干燥的Cl2通过有色鲜花 | 鲜花褪色 | Cl2有漂白性 |
| C | 向某无色溶液中滴加氯水和CCl4,振荡、静置 | 下层溶液显紫色 | 原溶液中有I- |
| D | 取久置的Na2O2粉末,向其中滴加过量的盐酸 | 产生气体 | Na2O2没有变质 |
| A. | A | B. | B | C. | C | D. | D |
13.如图装置可以用来发生、洗涤、干燥、收集(不考虑尾气处理)气体.该装置可用于( )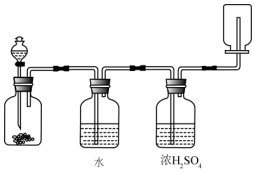

| A. | 锌和盐酸生成氢气 | B. | 氯酸钾和二氧化锰生成氧气 | ||
| C. | 碳酸钙和盐酸生成二氧化碳 | D. | 氯化钠和浓硫酸生成氯化氢 |
