题目内容
A、B、C、D、E、F 6种主族元素,它们的原子序数依次增大.已知A、C、F三种元素的原子最外层共有10个电子,且这三种元素的最高价氧化物的水化物之间能两两发生反应都生成盐和水;又知D元素的原子最外层电子数比次外层电子数少4,E元素原子的次外层电子数比最外层电子数多3.请填写下列空白处:
(1)元素的符号:A.
(2)元素B和F形成的化合物的电子式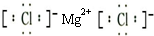
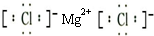 .
.
(3)D元素的氧化物属于
(4)E元素的最高价氧化物与水反应的化学方程式是
(1)元素的符号:A.
Na
Na
,C.Al
Al
.(2)元素B和F形成的化合物的电子式
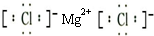
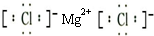
(3)D元素的氧化物属于
原子
原子
晶体,含a mol D的上述晶体中含D-O共价键4a
4a
mol.(4)E元素的最高价氧化物与水反应的化学方程式是
P2O5+3H2O=2H3PO4
P2O5+3H2O=2H3PO4
.分析:A、B、C、D、E、F 6种主族元素,它们的原子序数依次增大.已知A、C、F三种元素的原子最外层共有10个电子,且这三种元素的最高价氧化物的水化物之间能两两发生反应都生成盐和水,则C为Al,故A为Na,B为Mg元素;F的最外层电子数为10-1-3=6,则F为硫元素;D元素的原子最外层电子数比次外层电子数少4,则D为Si元素,E元素原子的次外层电子数比最外层电子数多3,则E为P元素,据此解答.
解答:解:A、B、C、D、E、F 6种主族元素,它们的原子序数依次增大.已知A、C、F三种元素的原子最外层共有10个电子,且这三种元素的最高价氧化物的水化物之间能两两发生反应都生成盐和水,则C为Al,故A为Na,B为Mg元素;F的最外层电子数为10-1-3=6,则F为硫元素;D元素的原子最外层电子数比次外层电子数少4,则D为Si元素,E元素原子的次外层电子数比最外层电子数多3,则E为P元素,
(1)由上述分析可知,A为Na元素,C为Al元素,
故答案为:Na;Al;
(2)元素B和F形成的化合物为MgCl2,由镁离子与氯离子构成,其电子式为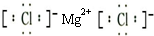 ,
,
故答案为: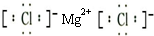 ;
;
(3)D元素的氧化物为SiO2,属于原子晶体,晶体中每个硅原子形成4个Si-O键,含a mol D的上述晶体中含SiD-O共价键4a mol,
故答案为:原子;4a;
(4)E元素的最高价氧化物为五氧化二磷,与水反应的化学方程式为P2O5+3H2O=2H3PO4,
故答案为:P2O5+3H2O=2H3PO4.
(1)由上述分析可知,A为Na元素,C为Al元素,
故答案为:Na;Al;
(2)元素B和F形成的化合物为MgCl2,由镁离子与氯离子构成,其电子式为
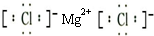 ,
,故答案为:
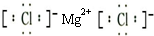 ;
;(3)D元素的氧化物为SiO2,属于原子晶体,晶体中每个硅原子形成4个Si-O键,含a mol D的上述晶体中含SiD-O共价键4a mol,
故答案为:原子;4a;
(4)E元素的最高价氧化物为五氧化二磷,与水反应的化学方程式为P2O5+3H2O=2H3PO4,
故答案为:P2O5+3H2O=2H3PO4.
点评:本题考查元素推断、常用化学用语、物质结构与性质等,难度不大,注意基础知识的理解掌握.

练习册系列答案
 教材全解字词句篇系列答案
教材全解字词句篇系列答案
相关题目
 [化学/选修/物质结构与性质]A、B、C、D、E五种短周期元素,原子序数依次增大,各元素对应的单质均为固体.A、C、E三元素的原子核外均只有2个未成对电子.B、E元素的原子序数之和等于C、D元素的原子序数之和.
[化学/选修/物质结构与性质]A、B、C、D、E五种短周期元素,原子序数依次增大,各元素对应的单质均为固体.A、C、E三元素的原子核外均只有2个未成对电子.B、E元素的原子序数之和等于C、D元素的原子序数之和.