题目内容
15.下列物质中,既含有离子键,又含有共价键的是( )| A. | H2O | B. | CaCl2 | C. | CaO2 | D. | Cl2 |
分析 一般来说,活泼金属元素与活泼非金属元素形成离子键,非金属元素之间形成共价键,以此来解答.
解答 解:A.水中只含共价键,故A不选;
B.CaCl2中只含离子键,故B不选;
C.CaO2中含离子键,过氧根中存在共价键,故C选;
D.Cl2中只含共价键,故D不选.
故选:C.
点评 本题考查化学键,为高频考点,把握离子键、共价键判断的一般规律为解答的关键,注意特殊物质中的化学键(氯化铝、铵盐等),题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
5.下列物质的电子式书写正确的是( )
| A. | 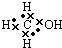 | B. | 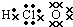 | C. | 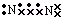 | D. | 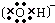 |
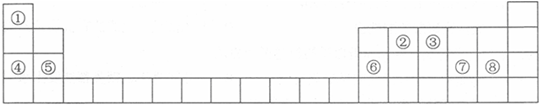
10.已知元素A~E表示元素周期表中短周期的四种元素,请根据表中信息回答下列问题.
(1)A在元素周期表中的位置为第二周期第ⅣA族,元素A的一种同位素可测定文物年代,这种同位素的符号是146C.比较B、D、E的离子半径的大小S2->O2->Na+(用离子符号表示).
(2)用电子式表示元素B形成的10e-的氢化物分子的形成过程 .
.
(3)已知E在B的单质中燃烧生成淡黄色的固体,该固体化合物的电子式为 .
.
(4)C的氢化物和C的最高价氧化物的水化物反应生成甲,甲是离子化合物(填“共价化合物”或“离子化合物”),甲中的化学键类型为离子键、共价键.
(5)请写出 A的单质与D的最高价含氧酸反应的化学方程式:C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+2SO2↑+2H2O
(6)元素D的气态氢化物与过氧化氢溶液混合后有浅黄色固体生成,请写出发生的化学方程式H2O2+H2S=S↓+2H2O.
| 元素 | 性质或结构信息 |
| A | 组成有机物的必须元素 |
| B | 原子最外层电子数是电子层数的3倍. |
| C | 工业上通过分离液态空气获得其单质.原子的最外层电子数是内层电子总数的2.5倍. |
| D | 单质是黄色晶体,不溶于水,微溶于酒精,易溶于二硫化碳,游离态的D存在于火山喷口附近或地壳的岩层里. |
| E | 最高价氧化物的水化物能电离出与Ne电子数相等的阴阳离子. |
(2)用电子式表示元素B形成的10e-的氢化物分子的形成过程
 .
.(3)已知E在B的单质中燃烧生成淡黄色的固体,该固体化合物的电子式为
 .
.(4)C的氢化物和C的最高价氧化物的水化物反应生成甲,甲是离子化合物(填“共价化合物”或“离子化合物”),甲中的化学键类型为离子键、共价键.
(5)请写出 A的单质与D的最高价含氧酸反应的化学方程式:C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+2SO2↑+2H2O
(6)元素D的气态氢化物与过氧化氢溶液混合后有浅黄色固体生成,请写出发生的化学方程式H2O2+H2S=S↓+2H2O.
7.下列有关说法正确的是( )
| A. | 石油的组成元素主要是碳和氧,同时还含有少量的硫、氢、氮等 | |
| B. | 煤是由有机物和无机物所组成的复杂的混合物,煤中含量最高的元素是氢 | |
| C. | 甲烷在一定条件下可被氧化,生成的混合气体在催化剂和一定压强、温度下能合成甲醇(CH3OH) | |
| D. | 所有烷烃中都存在碳碳单键 |
4.下列有关脂肪烃的组成和性质归纳正确的是( )
| A. | 脂肪烃都能使溴水、酸性高锰酸钾溶液褪色 | |
| B. | 脂肪烃随碳原子数增多,氢元素的质量分数减小 | |
| C. | 脂肪烃密度都小于水的密度,都能发生氧化反应 | |
| D. | 脂肪烃的一氯代物都有两种或两种以上的结构 |
5.为除去括号内杂质,下列有关试剂和操作方法不正确的是( )
| A. | 溴苯(苯):蒸馏 | B. | 苯(苯酚):加溴水振荡后,过滤 | ||
| C. | 乙烷(乙烯):溴水,洗气 | D. | 苯(溴):稀NaOH溶液,分液 |
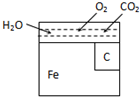 金属材料在使用的过程中,由于长期暴露在空气中,会因为氧化而逐渐腐蚀.其中电化学腐蚀是金属的主要形式.右图是钢铁在空气中发生电化学腐蚀的简单图示.试分析下列问题:钢铁发生电化腐蚀时,可以形成原电池.
金属材料在使用的过程中,由于长期暴露在空气中,会因为氧化而逐渐腐蚀.其中电化学腐蚀是金属的主要形式.右图是钢铁在空气中发生电化学腐蚀的简单图示.试分析下列问题:钢铁发生电化腐蚀时,可以形成原电池.