题目内容
5.下列物质的电子式书写正确的是( )| A. | 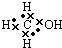 | B. | 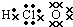 | C. | 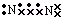 | D. | 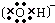 |
分析 A.甲醇为共价化合物,根据其结构式书写;B.HClO为共价化合物,分子中存在1个氧氢键和1个Cl-O键;C.氮气分子中存在氮氮三键,氮原子最外层为8电子;据此书写即可;D.电子式是用原子的最外层电子表示出来的式子.
解答 解:A.甲醇为共价化合物,其结构式为 ,每一个短线代表一对电子,则其电子式为:
,每一个短线代表一对电子,则其电子式为: ,故A错误;B.HClO为共价化合物,分子中存在1个氧氢键和1个Cl-O键,次氯酸的电子式为:
,故A错误;B.HClO为共价化合物,分子中存在1个氧氢键和1个Cl-O键,次氯酸的电子式为: ,故B错误;C.氮气的电子式为
,故B错误;C.氮气的电子式为 ,故C错误;D.电子式是用原子的最外层电子表示出来的式子,故羟基的电子式为
,故C错误;D.电子式是用原子的最外层电子表示出来的式子,故羟基的电子式为 ,故D正确,故选D.
,故D正确,故选D.
点评 本题主要考查的是电子式的书写,难度不大,需要掌握共价化合物以及离子化合物的区别.

练习册系列答案
相关题目
16.下列有机物不是同一种物质的是( )
| A. | 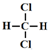 和 和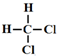 | B. | CH2=CH-CH=CH2和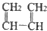 | ||
| C. | C(CH3)3C(CH3)3和CH3(CH2)3C(CH3)3 | D. | 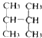 和 和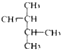 |
13.下列叙述错误的是( )
| A. | ⅡA族元素的阳离子与上周期稀有气体元素的原子具有相同的核外电子排布 | |
| B. | 元素周期表中从ⅢB族到ⅡB族10个纵行的元素都是金属元素 | |
| C. | 多电子原子中,在离核较近的区域内运动的电子能量较低 | |
| D. | 两个非金属元素原子间只可能形成共价键,而含金属元素的化合物中一定含离子键 |
10.下列说法中错误的是( )
| A. | KAl(SO4)2•12H2O不属于配合物 | |
| B. | 配位化合物中的配体可以是分子也可以是阴离子 | |
| C. | 配位数为4的配合物均为正四面体结构 | |
| D. | 已知[Cu(NH3)2]2+的空间构型为直线型,则它的中心原子采用sp杂化 |
17.用NA表示阿伏加德罗常数的值.下列说法正确的是( )
| A. | 32 g氧气和臭氧(O3)混合气体中含有氧原子的数目为2NA | |
| B. | 标准状况下,4.48 L水中含有H2O分子的数目为0.2NA | |
| C. | 1 mol铁与足量的硝酸反应,生成H2分子的数目为NA | |
| D. | 0.2 mol•L-1 CaCl2溶液中含有Cl-离子的数目为0.4NA |
14.制造玻璃的主要原料( )
| A. | 烧碱 石灰石 石英 | B. | 纯碱 石灰石 石英 | ||
| C. | 纯碱 生石灰 石英 | D. | 纯碱 熟石灰 石英 |
15.下列物质中,既含有离子键,又含有共价键的是( )
| A. | H2O | B. | CaCl2 | C. | CaO2 | D. | Cl2 |
