题目内容
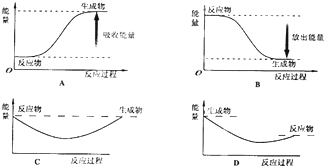
(1)若适量的N2和O2完全反应,每生成23克NO2需要吸收16.95kJ的热量.写出该反应的热化学方程式 .
(2)若25℃,101kPa下,1g CH4完全燃烧生成液态水和CO2气体,放出55.6kJ的热量,则甲烷的燃烧热为 .
(2)若25℃,101kPa下,1g CH4完全燃烧生成液态水和CO2气体,放出55.6kJ的热量,则甲烷的燃烧热为
考点:热化学方程式,燃烧热
专题:化学反应中的能量变化
分析:(1)根据热化学方程式的以及结合书写方法来回答;
(2)燃烧热是指在25℃、101kPa下,1mol纯净物完全燃烧生成稳定的氧化物放出的热量,表示燃烧热的热化学方程式中可燃物的物质的量必须为1mol,产物必须为稳定氧化物.
(2)燃烧热是指在25℃、101kPa下,1mol纯净物完全燃烧生成稳定的氧化物放出的热量,表示燃烧热的热化学方程式中可燃物的物质的量必须为1mol,产物必须为稳定氧化物.
解答:
解:(1)适量的N2和O2完全反应,每生成23克NO2需要吸收16.95kJ热量,所以每生成92克NO2需要吸收67.8kJ热量,则热化学方程式为:N2(g)+2O2(g)=2NO2(g)△H=67.8kJ?mol-1,
故答案为:N2(g)+2O2(g)=2NO2(g)△H=67.8kJ?mol-1;
(2)1g CH4完全燃烧生成液态水和CO2气体,放出55.6kJ的热量,则1mol即16g CH4完全燃烧生成液态水和CO2气体,16×55.6kJ=889.6kJ,则甲烷燃烧热的热化学方程式为:CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-889.6KJ?mol-1,
故答案为:CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-889.6KJ?mol-1.
故答案为:N2(g)+2O2(g)=2NO2(g)△H=67.8kJ?mol-1;
(2)1g CH4完全燃烧生成液态水和CO2气体,放出55.6kJ的热量,则1mol即16g CH4完全燃烧生成液态水和CO2气体,16×55.6kJ=889.6kJ,则甲烷燃烧热的热化学方程式为:CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-889.6KJ?mol-1,
故答案为:CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-889.6KJ?mol-1.
点评:本题主要考查了热化学方程式的书写,注意热化学方程式的意义是解题的关键,难度不大.

练习册系列答案
相关题目
下列各组离子中,能在溶液中大量共存的是( )
| A、H+、Cu2+、OH-、NO3- |
| B、H+、K+、Cl-、ClO- |
| C、Fe3+、Na+、Cl-、SO42- |
| D、Na+、Ba2+、SO42-、OH- |
下列说法中正确的是( )
| A、胶体区别于其它分散系的本质特性是丁达尔现象 |
| B、在豆浆里加入盐卤做豆腐与胶体的聚沉有关 |
| C、Fe(OH)3胶体带正电荷 |
| D、Fe(OH)3胶体制备可以通过将饱和FeCl3溶液逐滴滴入NaOH浓溶液中 |
 根据下列叙述写出相应的热化学方程式:
根据下列叙述写出相应的热化学方程式: