题目内容
火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂液态过氧化氢(H2O2).当把0.4mol液态肼和0.8mol H2O2混合反应,生成氮气和水蒸气,放出256.7kJ的热量(相当于25℃、101kPa下测得的热量).
又知H2O(l)=H2O(g)△H=+44kJ/mol.
(1)写出过氧化氢(H2O2)的结构式 .
(2)液态肼与液态过氧化氢反应生成液态水反应的热化学方程式为 .
(3)此反应用于火箭推进,除释放大量热和快速产生大量气体外,还有一个很大的优点是 .
又知H2O(l)=H2O(g)△H=+44kJ/mol.
(1)写出过氧化氢(H2O2)的结构式
(2)液态肼与液态过氧化氢反应生成液态水反应的热化学方程式为
(3)此反应用于火箭推进,除释放大量热和快速产生大量气体外,还有一个很大的优点是
考点:热化学方程式
专题:化学反应中的能量变化
分析:(1)过氧化氢分子式H2O2,每个氧原子形成两个共价键,依据结构写出物质的结构式;
(2)依据热化学方程式和盖斯定律计算得到热化学方程式,得到反应的焓变;
(3)肼燃烧生成氮气和水;
(2)依据热化学方程式和盖斯定律计算得到热化学方程式,得到反应的焓变;
(3)肼燃烧生成氮气和水;
解答:
解:(1)过氧化氢分子式H2O2,每个氧原子形成两个共价键,分子结构为: ;
;
故答案为: ;
;
(2)0.4mol液态肼与足量过氧化氢反应,生成氮气和水蒸气,放出256.7kJ的热量,32g肼燃烧放热641.625kJ;肼燃烧的热化学方程式为:
N2H4(l)+2H2O2(l)═N2(g)+4H2O(g)△H=-641.75kJ/mol;
①N2H4(l)+2H2O2(l)═N2(g)+4H2O(g)△H=-641.75kJ/mol,
②H2O(l)═H2O(g)△H=+44kJ/mol;
依据盖斯定律,①-②×4得到:N2H4(l)+2H2O2(l)═N2(g)+4H2O(l)△H=-817.75kJ/mol
故答案为:N2H4(l)+2H2O2(l)═N2(g)+4H2O(l)△H=-817.75kJ/mol;
(3)肼燃烧生成氮气和水,除释放大量热和快速产生大量气体外,生成的物质无污染;
故答案为:生成N2和H2O,对环境无污染;
 ;
;故答案为:
 ;
;(2)0.4mol液态肼与足量过氧化氢反应,生成氮气和水蒸气,放出256.7kJ的热量,32g肼燃烧放热641.625kJ;肼燃烧的热化学方程式为:
N2H4(l)+2H2O2(l)═N2(g)+4H2O(g)△H=-641.75kJ/mol;
①N2H4(l)+2H2O2(l)═N2(g)+4H2O(g)△H=-641.75kJ/mol,
②H2O(l)═H2O(g)△H=+44kJ/mol;
依据盖斯定律,①-②×4得到:N2H4(l)+2H2O2(l)═N2(g)+4H2O(l)△H=-817.75kJ/mol
故答案为:N2H4(l)+2H2O2(l)═N2(g)+4H2O(l)△H=-817.75kJ/mol;
(3)肼燃烧生成氮气和水,除释放大量热和快速产生大量气体外,生成的物质无污染;
故答案为:生成N2和H2O,对环境无污染;
点评:本题考查了化学反应能量变化的计算应用,物质结构分析判断,盖斯定律的计算,热化学方程式书写方法,题目难度中等.

练习册系列答案
 中考利剑中考试卷汇编系列答案
中考利剑中考试卷汇编系列答案 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案
相关题目
下列过程中,共价键被破坏的是( )
| A、HCl气体溶于水 |
| B、酒精溶于水 |
| C、冰融化成水 |
| D、碘升华 |
 普通水泥在固化过程中自由水分子减少并产生Ca(OH)2使溶液呈碱性.根据这一物理化学特点,科学家发明了电动势法测水泥初凝时间.此方法的原理如图所示,反应的总方程式为:2Cu+Ag2O═2CuO+2Ag,下列有关说法正确的是( )
普通水泥在固化过程中自由水分子减少并产生Ca(OH)2使溶液呈碱性.根据这一物理化学特点,科学家发明了电动势法测水泥初凝时间.此方法的原理如图所示,反应的总方程式为:2Cu+Ag2O═2CuO+2Ag,下列有关说法正确的是( )| A、电池工作时,OH-向正极移动 |
| B、测量原理示意图中,Ag2O为负极 |
| C、电流方向是从Ag2O/Ag电极到Cu电极 |
| D、正极的电极反应为:2Cu+2OH--2e-═Cu2O+H2O |
在标准状况下,由甲烷、甲醛和乙烷组成的11.2L混合气体完全燃烧后,生成15.68L相同状况下的CO2气体.则混合气体中乙烷的体积分数为( )
| A、20% | B、40% |
| C、60% | D、80% |
化学与环境、材料、信息、能源关系密切,下列说法正确的是( )
| A、半导体行业中有一句话:“从沙滩到用户”,计算机芯片的材料是二氧化硅 |
| B、绿色化学的核心是利用化学原理治理环境污染 |
| C、将煤气化或液化,获得清洁燃料 |
| D、PM2.5是指大气中直径接近于2.5×10-6m的颗粒物,也称细颗粒物,这些细颗粒物分散在空气中形成混合物具有丁达尔效应 |
25℃时,下列有关溶液中微粒的物质的量浓度关系不正确的是( )
| A、0.1 mol?L-1 (NH4)2Fe(SO4)2溶液中:c(SO42-)>c(NH4+)>c(Fe2+)>c(H+) |
| B、pH=11的氨水和pH=3的盐酸溶液等体积混合,所得溶液中:c(Cl-)>c(NH4+)>c(OH-)>c(H+) |
| C、0.1 mol?L-1 CH3COONa溶液中:c(CH3COO-)+c(CH3COOH)=0.1 mol?L-1 |
| D、0.1 mol?L-1的醋酸钠溶液20 mL与0.1 mol?L-1盐酸10 mL混合后溶液显酸性:c(CH3COO-)>c(Cl-)>c(CH3COOH)>c(H+) |
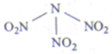 科学家最近研制出可望成为高效火箭液态推进剂的N(NO2)3(如图所示).已知该分子中N-N-N键角都是108.1°,用NA表示阿伏加德罗常数,下列有关N(NO2)3的说法正确的是]( )
科学家最近研制出可望成为高效火箭液态推进剂的N(NO2)3(如图所示).已知该分子中N-N-N键角都是108.1°,用NA表示阿伏加德罗常数,下列有关N(NO2)3的说法正确的是]( )| A、分子中四个氮原子共平面 |
| B、7.6 g N(NO2)3和N2O3混合物中共含氮原子数为0.2NA |
| C、标准状况下,2.24L N(NO2)3含有的分子数为0.1NA |
| D、15.2g该物质含有0.6NA个非极性键 |