题目内容
在一密闭容器中有A、B两种气体,开始时浓度分别为amol?L-1、bmol?L-1,A跟B反应生成C,方程式为:A+2B?3C.t秒末时,用C表示的反应速率为dmol?L-1?S-1,则此时B的浓度为多少mol?L-1?
考点:反应速率的定量表示方法
专题:化学反应速率专题
分析:依据化学平衡三段式列式计算,根据三段式计算出各组分物质的量浓度变化量、平衡时物质的量浓度,以此计算c(B).
解答:
解:A、B两种气体,开始时浓度分别为amol?L-1、bmol?L-1,t秒末时,用C表示的反应速率为dmol?L-1?S-1,依据反应速率计算反应生成的物质C的量浓度C(C)=△V×△t=dmol?L-1?S-1×tS=dtmol?L-1;
A+2B?3C
起始量(mol?L-1) a b 0
变化量(mol?L-1)
dt
dt dt
平衡量(mol?L-1)(a-
dt) (b-
dt) dt
c(B)=(b-
dt)mol?L-1;
答:(b-
dt)mol?L-1.
A+2B?3C
起始量(mol?L-1) a b 0
变化量(mol?L-1)
| 1 |
| 3 |
| 2 |
| 3 |
平衡量(mol?L-1)(a-
| 1 |
| 3 |
| 2 |
| 3 |
c(B)=(b-
| 2 |
| 3 |
答:(b-
| 2 |
| 3 |
点评:本题考查化学平衡的计算,题目难度不大,注意对速率公式的理解与灵活运用,注意三段式应用.

练习册系列答案
相关题目
 普通水泥在固化过程中自由水分子减少并产生Ca(OH)2使溶液呈碱性.根据这一物理化学特点,科学家发明了电动势法测水泥初凝时间.此方法的原理如图所示,反应的总方程式为:2Cu+Ag2O═2CuO+2Ag,下列有关说法正确的是( )
普通水泥在固化过程中自由水分子减少并产生Ca(OH)2使溶液呈碱性.根据这一物理化学特点,科学家发明了电动势法测水泥初凝时间.此方法的原理如图所示,反应的总方程式为:2Cu+Ag2O═2CuO+2Ag,下列有关说法正确的是( )| A、电池工作时,OH-向正极移动 |
| B、测量原理示意图中,Ag2O为负极 |
| C、电流方向是从Ag2O/Ag电极到Cu电极 |
| D、正极的电极反应为:2Cu+2OH--2e-═Cu2O+H2O |
在标准状况下,由甲烷、甲醛和乙烷组成的11.2L混合气体完全燃烧后,生成15.68L相同状况下的CO2气体.则混合气体中乙烷的体积分数为( )
| A、20% | B、40% |
| C、60% | D、80% |
25℃时,下列有关溶液中微粒的物质的量浓度关系不正确的是( )
| A、0.1 mol?L-1 (NH4)2Fe(SO4)2溶液中:c(SO42-)>c(NH4+)>c(Fe2+)>c(H+) |
| B、pH=11的氨水和pH=3的盐酸溶液等体积混合,所得溶液中:c(Cl-)>c(NH4+)>c(OH-)>c(H+) |
| C、0.1 mol?L-1 CH3COONa溶液中:c(CH3COO-)+c(CH3COOH)=0.1 mol?L-1 |
| D、0.1 mol?L-1的醋酸钠溶液20 mL与0.1 mol?L-1盐酸10 mL混合后溶液显酸性:c(CH3COO-)>c(Cl-)>c(CH3COOH)>c(H+) |
下列说法正确的是( )
| A、双氧水被称为绿色氧化剂,是因为其还原产物为O2,对环境没有污染 |
| B、新制备的氯水中只存在三种分子、三种离子 |
| C、10mL质量分数为98%的H2SO4,用水稀释至100mL,H2SO4的质量分数为9.8% |
| D、浓硝酸与浓盐酸一样,在空气中出现白雾 |
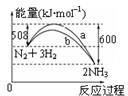 根据下列叙述写出相应的热化学方程式:
根据下列叙述写出相应的热化学方程式: