题目内容
 根据下列叙述写出相应的热化学方程式:
根据下列叙述写出相应的热化学方程式:(1)已知16g固体硫完全燃烧时放出148.4kJ的热量,该反应的热化学方程式是
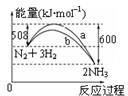
(2)如图是298K时N2与H2反应过程中能量变化的曲线图.该反应的热化学方程式为:
考点:热化学方程式
专题:化学反应中的能量变化
分析:(1)根据热化学方程式的书写方法可知,化学计量数与反应热成正比,并注意标明物质的聚集状态来解答;
(2)图象分析可知是1molN2与和3molH2完全反应生成2molNH3,反应是放热反应,反应的焓变△H=508kJ/mol-600kJ/mol=-92kJ/mol,据此写出反应的热化学方程式.
(2)图象分析可知是1molN2与和3molH2完全反应生成2molNH3,反应是放热反应,反应的焓变△H=508kJ/mol-600kJ/mol=-92kJ/mol,据此写出反应的热化学方程式.
解答:
解:(1)16g固体硫完全燃烧时放出148.4kJ的热量,即1molS完全燃烧时放出放出296.8kj热量,则热化学方程式为:S(s)+O2(g)=SO2(g);△H=-296.8 kJ/mol,
故答案为:S(s)+O2(g)=SO2(g);△H=-296.8 kJ/mol;
(2)图象分析可知,图象中表示的是1molN2与和3molH2氧气完全反应生成2molNH3,反应是放热反应,反应的焓变△H=508kJ/mol-600kJ/mol=-92kJ/mol,反应的热化学方程式为:N2(g)+3H2(g)?2NH3(g)△H=-92 kJ?mol-1 ,
故答案为:N2(g)+3H2(g)?2NH3(g)△H=-92 kJ?mol-1.
故答案为:S(s)+O2(g)=SO2(g);△H=-296.8 kJ/mol;
(2)图象分析可知,图象中表示的是1molN2与和3molH2氧气完全反应生成2molNH3,反应是放热反应,反应的焓变△H=508kJ/mol-600kJ/mol=-92kJ/mol,反应的热化学方程式为:N2(g)+3H2(g)?2NH3(g)△H=-92 kJ?mol-1 ,
故答案为:N2(g)+3H2(g)?2NH3(g)△H=-92 kJ?mol-1.
点评:本题考查化学反应中的能量变化及利用盖斯定律确定反应及其能量的关系,注意键能计算焓变的方法,题目难度中等,注重基础知识的考查.

练习册系列答案
相关题目
对化学方程式C+2CuO
2Cu+CO2↑理解不正确的是( )
| ||
| A、木炭与氧化铜在高温下反应生成铜和二氧化碳 |
| B、12份质量的碳可与160份质量的氧化铜在高温下反应生成128份质量的铜和44份质量的二氧化碳 |
| C、若以NA代表6.02×1023个粒子,则NA个碳原子与2NA个氧化铜分子在高温下反应,生成2NA个铜原子和NA个二氧化碳分子 |
| D、一个碳原子和两个氧化铜分子高温加热时可生成两个铜原子和一个二氧化碳分子 |
下列过程中,共价键被破坏的是( )
| A、HCl气体溶于水 |
| B、酒精溶于水 |
| C、冰融化成水 |
| D、碘升华 |
下列生产、生活情境都涉及能量转化和利用,其中不发生化学变化的是( )
A、 海水晒盐 |
B、 天然气燃烧 |
C、 闪电时产生氮氧化物 |
D、 原电池放电 |
 普通水泥在固化过程中自由水分子减少并产生Ca(OH)2使溶液呈碱性.根据这一物理化学特点,科学家发明了电动势法测水泥初凝时间.此方法的原理如图所示,反应的总方程式为:2Cu+Ag2O═2CuO+2Ag,下列有关说法正确的是( )
普通水泥在固化过程中自由水分子减少并产生Ca(OH)2使溶液呈碱性.根据这一物理化学特点,科学家发明了电动势法测水泥初凝时间.此方法的原理如图所示,反应的总方程式为:2Cu+Ag2O═2CuO+2Ag,下列有关说法正确的是( )| A、电池工作时,OH-向正极移动 |
| B、测量原理示意图中,Ag2O为负极 |
| C、电流方向是从Ag2O/Ag电极到Cu电极 |
| D、正极的电极反应为:2Cu+2OH--2e-═Cu2O+H2O |
 根据下列叙述写出相应的热化学方程式:
根据下列叙述写出相应的热化学方程式: