题目内容
5.下列叙述或离子方程式书写正确的是( )| A. | 将少量二氧化硫通入次氯酸钠溶液中:SO2+H2O+3ClO-═SO42-+Cl-+2HClO | |
| B. | 向含有Fe2O3悬浊液中通入HI气体:Fe2O3+6H+═2Fe3++3H2O | |
| C. | 用惰性电极电解MgCl2溶液:2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$Cl2↑+H2↑+2OH- | |
| D. | 等物质的量的Ba(OH)2与(NH4)2Fe(SO4)2在溶液中反应:Ba2++2OH-+2NH4++SO42-═BaSO4↓+2NH3•H2O |
分析 A.二氧化硫能够被次氯酸根氧化生成硫酸根离子;
B.三价铁离子能够氧化碘离子生成单质碘;
C.氢氧化镁为沉淀应保留化学式;
D.等物质的量的Ba(OH)2与NH4HSO4在稀溶液中反应,铵离子与氢氧根离子恰好反应.
解答 解:A.将少量二氧化硫通入次氯酸钠溶液中,离子方程式:SO2+H2O+3ClO-═SO42-+Cl-+2HClO,故A正确;
B.氧化铁可溶于氢碘酸,三价铁具有氧化性能氧化碘离子,反应的离子方程式为:Fe2O3+2I-+6H+=2Fe2++3H2O+I2,故B错误;
C.用惰性电极电解MgCl2溶液的离子反应为Mg2++2Cl-+2H2O$\frac{\underline{\;通电\;}}{\;}$Mg(OH)2↓+O2↑+H2↑,故C错误;
D.等物质的量的Ba(OH)2与(NH4)2Fe(SO4)2在溶液中反应,离子方程式:Ba2++2OH-+H++NH4++SO42-=BaSO4↓+H2O+NH3?H2O,故D错误;
故选:A.
点评 本题考查离子方程式的书写,明确离子方程式书写方法及反应实质是解题关键,注意反应物用量对反应的影响,选项D为易错选项.

练习册系列答案
相关题目
15.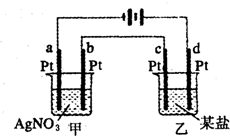 如图所示的装置,两烧杯中均为相应的水溶液,通电一段时间后,测得甲池中某电极质量增加2.16g,乙池中某电极上析出0.24g某金属,下列说法正确的是( )
如图所示的装置,两烧杯中均为相应的水溶液,通电一段时间后,测得甲池中某电极质量增加2.16g,乙池中某电极上析出0.24g某金属,下列说法正确的是( )
 如图所示的装置,两烧杯中均为相应的水溶液,通电一段时间后,测得甲池中某电极质量增加2.16g,乙池中某电极上析出0.24g某金属,下列说法正确的是( )
如图所示的装置,两烧杯中均为相应的水溶液,通电一段时间后,测得甲池中某电极质量增加2.16g,乙池中某电极上析出0.24g某金属,下列说法正确的是( )| A. | 某盐溶液可能是Mg(NO3)2溶液 | |
| B. | 甲池是a极上析出金属银,乙池是d极上析出某金属 | |
| C. | 甲池是b极上析出金属银,乙池是c极上析出某金属 | |
| D. | 某盐溶液可能是CuSO4溶液 |
16.下列说法正确的是( )
| A. | 物质发生化学反应时必然伴随着能量变化 | |
| B. | 金属铜导电,故金属铜是电解质 | |
| C. | 自发反应都是熵增大的反应 | |
| D. | 增大反应物浓度,可增大单位体积内活化分子的百分数,从而使反应速率增大 |
13.下列对应化学反应的离子方程式书写正确的是( )
| A. | 铜与硝酸银溶液反应:Cu+Ag+═Cu2++Ag | |
| B. | 铁在氯气中燃烧:2Fe+3Cl2═2Fe3++6Cl- | |
| C. | 硫酸铜溶液中滴加氢氧化钡溶液:SO42-+Ba2+═BaSO4↓ | |
| D. | 氧化铝与稀盐酸混合:Al2O3+6H+═2Al3++3H2O |
10.下列各物质,能由单质间发生化合反应得到,但不能由单质与酸发生置换反应得到的是( )
| A. | MgCl2 | B. | FeCl2 | C. | AlCl3 | D. | CuCl2 |
17.室温下,取浓度相同的NaOH和HCl溶液,以3:1体积比相混合,所得溶液的pH等于12,则原溶液的浓度为( )
| A. | 0.01 mol/L | B. | 0.02 mol/L | C. | 0.05 mol/L | D. | 0.06 mol/L |
14.ABn型分子中,若A原子的最外层未达到稳定结构,则该分子被称为缺电子分子.下列分子属于缺电子分子的是( )
| A. | CO2 | B. | BeCl2 | C. | BF3 | D. | XeF2 |
5.下列对实验操作的叙述错误的是( )
| A. | 用胶头滴管加液时,不能伸入试管中 | |
| B. | 蒸馏盛在烧瓶中含水的酒精,需在瓶内放一些碎瓷片 | |
| C. | 萃取实验中涉及气体压强原理 | |
| D. | 用容积为100 mL的量筒量取80 mL无水乙醇,使液面最低点至刻度80 mL处 |
