题目内容
6.生活离不开水.净化水的知识在日常生活中有着广泛的应用.(1)茶杯内的纱网,可将茶叶与茶水分离,便于饮用,该设计利用的化学原理是过滤
(2)自制净水器中常加入活性炭,用于除去水中的异味和色素.
(3)自来水厂用二氧化氯消毒杀菌,二氧化氯的化学式为ClO2.
(4)井水中含有较多的钙、镁离子,为降低硬度,可采用的方法是加热煮沸(或蒸馏).
分析 (1)茶杯内的纱网能滤去茶叶,和过滤器除去水中泥沙原理是一样的;
(2)能除去水中的异味和色素的物质必须有吸附性,常用的吸附剂是活性炭;
(3)写化学式通常将氧的元素符号写在右边,另一种元素的符号写在左方,在元素符号右下角标上原子个数即可,所以二氧化氯的化学式为ClO2;
(4)较为常用的将硬水软化的方法有加热煮沸或蒸馏.
解答 解:(1)茶杯内的纱网能滤去茶叶,和过滤器除去水中泥沙原理是一样的,则将茶叶与茶水分离原理为过滤,故答案为:过滤;
(2)能除去水中的异味和色素的物质必须有吸附性,常用的吸附剂是活性炭,故答案为:活性炭;
(3)写化学式通常将氧的元素符号写在右边,另一种元素的符号写在左方,在元素符号右下角标上原子个数即可,所以二氧化氯的化学式为ClO2,故答案为:ClO2;
(4)井水中含有较多的钙、镁离子,为降低硬度,可采用的方法是有加热煮沸或蒸馏,故答案为:加热煮沸(或蒸馏).
点评 本题考查混合物分离提纯,为高频考点,把握物质的性质、性质差异及混合物分离方法为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
17.短周期主族元素X、Y、Z、W在元素周期表中的相对位置如下图示.已知X的最低负价与Y的最高正价代数和为零,下列说法正确的是( )
| X | ||||
| Y | Z | W |
| A. | X分别与Y、Z形成的化合物中化学键类型相同 | |
| B. | Z的最高价氧化物的水化物酸性比W的强 | |
| C. | X的简单气态氢化物的稳定性比W的弱 | |
| D. | 原子半径的大小顺序:r(Y)>r(Z)>r(W)>r(X) |
14.常温下,下列各组离子在相应的条件下可能大量共存的是( )
| A. | 能使pH试纸变红的溶液中:CO32-、K+、Cl-、Na+ | |
| B. | $\frac{{K}_{W}}{c({H}^{+})}$═10-10mol/L的溶液中:Na+、HCO3-、Cl-、K+ | |
| C. | 在c(OH-)/c(H+)=1×1012的溶液中:NH4+、Fe2+、Cl-、NO3- | |
| D. | 由水电离产生的c(OH-)=1×10-12mol/L的溶液中:NO3-、Mg2+、Na+、SO42 |
1.下列离子方程式中,不正确的是( )
| A. | 浓烧碱溶液中加入铝片:A1+2OH-+2H2O═[A1(OH)4]-+H2↑ | |
| B. | 澄清石灰水与少量小苏打溶液混合:Ca2++OH-+HCO3一═CaCO3↓+H2O | |
| C. | 食醋和小苏打溶液混合;CH3COOH+HCO3一═CH3COO-十H2O+CO2↑ | |
| D. | 敞开体系,向FeC12溶液滴加NaOH溶液:4Fe2++8OH-+O2+2H2O═4Fe (OH)3↓ |
11.节能减排与我们的生活息息相关,参与节能减排是每一位公民应尽的义务.下列举措不符合这一要求的是( )
| A. | 推广使用乙醇汽油作为汽车的燃料 | |
| B. | 洗涤衣物时使用无磷洗衣粉等洗涤剂 | |
| C. | 尽量减少塑料购物袋的使用 | |
| D. | 加大石油、煤炭的开采速度,增加化石的供应量 |
18.在溶液中加入足量的过氧化钠后仍能大量共存的离子组是( )
| A. | K+、AlO2-、Cl-、SO42- | B. | H+、Ba2+、Cl-、NO3- | ||
| C. | Ca2+、Fe2+、NO3-、HCO3- | D. | Na+、Cl-、CO32-、HSO32- |
15.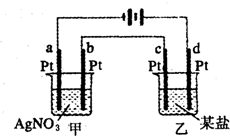 如图所示的装置,两烧杯中均为相应的水溶液,通电一段时间后,测得甲池中某电极质量增加2.16g,乙池中某电极上析出0.24g某金属,下列说法正确的是( )
如图所示的装置,两烧杯中均为相应的水溶液,通电一段时间后,测得甲池中某电极质量增加2.16g,乙池中某电极上析出0.24g某金属,下列说法正确的是( )
 如图所示的装置,两烧杯中均为相应的水溶液,通电一段时间后,测得甲池中某电极质量增加2.16g,乙池中某电极上析出0.24g某金属,下列说法正确的是( )
如图所示的装置,两烧杯中均为相应的水溶液,通电一段时间后,测得甲池中某电极质量增加2.16g,乙池中某电极上析出0.24g某金属,下列说法正确的是( )| A. | 某盐溶液可能是Mg(NO3)2溶液 | |
| B. | 甲池是a极上析出金属银,乙池是d极上析出某金属 | |
| C. | 甲池是b极上析出金属银,乙池是c极上析出某金属 | |
| D. | 某盐溶液可能是CuSO4溶液 |
16.下列说法正确的是( )
| A. | 物质发生化学反应时必然伴随着能量变化 | |
| B. | 金属铜导电,故金属铜是电解质 | |
| C. | 自发反应都是熵增大的反应 | |
| D. | 增大反应物浓度,可增大单位体积内活化分子的百分数,从而使反应速率增大 |