题目内容
已知H2(g)+
O2(g)=H2O(g);△H=-241.8kJ/mol.下列说法中不正确的是( )
| 1 |
| 2 |
| A、H2的燃烧热为-241.8kJ |
| B、2H2(g)+O2(g)=2H2O(g);△H=-483.6kJ/mol |
| C、1molH2完全燃烧生成液态水放出的热量大于241.8kJ |
| D、断开1molH2O的化学键吸收的总能量大于断裂1molH2和0.5 molO2的化学键所吸收的总能量 |
考点:反应热和焓变
专题:化学反应中的能量变化
分析:A.1mol可燃物燃烧生成稳定氧化物放出的热量为燃烧热;
B.热化学反应中,物质的量与反应放出的热量成正比;
C.气态水转化为液态水,需要吸收热量;
D.反应为放热反应,△H=反应物中键能之和-生成物中键能之和.
B.热化学反应中,物质的量与反应放出的热量成正比;
C.气态水转化为液态水,需要吸收热量;
D.反应为放热反应,△H=反应物中键能之和-生成物中键能之和.
解答:
解:A.1mol氢气燃烧生成稳定氧化物液态水放出的热量为燃烧热,本题生成的是水蒸气,故A错误;
B.热化学反应中,物质的量与反应放出的热量成正比,所以2H2(g)+O2(g)═2H2O(l)△H=-571.6 kJ/mol,故B正确;
C.气态水转化为液态水,能够释放热量,则1 mol H2完全燃烧生成液态水放出的热量大于241.8 kJ,故C正确;
D.反应为放热反应,△H=反应物中键能之和-生成物中键能之和,所以断开1 mol H2O的化学键吸收的总能量大于断裂1 mol H2和0.5 mol O2 的化学键所吸收的总能量,故D正确;
故选:A.
B.热化学反应中,物质的量与反应放出的热量成正比,所以2H2(g)+O2(g)═2H2O(l)△H=-571.6 kJ/mol,故B正确;
C.气态水转化为液态水,能够释放热量,则1 mol H2完全燃烧生成液态水放出的热量大于241.8 kJ,故C正确;
D.反应为放热反应,△H=反应物中键能之和-生成物中键能之和,所以断开1 mol H2O的化学键吸收的总能量大于断裂1 mol H2和0.5 mol O2 的化学键所吸收的总能量,故D正确;
故选:A.
点评:本题考查热化学反应,注意反应放出的热量与物质的状态、物质的物质的量有关,并注意键能与反应热的关系即可解答,题目难度不大.

练习册系列答案
相关题目
已知aXm+、bYn+、cXn-、dRm-四种离子的电子层结构相同(a、b、c、d为元素的核电荷数),则下列关系正确的是( )
| A、a-c=m-n |
| B、a-b=n-m |
| C、c-d=m+n |
| D、a-c=n+m |
某混合溶液中含氯化镁的浓度为2mol/L,含氯化铝的浓度为3mol/L,取此溶液200ml,为了使其中的Mg2+全部转化为Mg(OH)2沉淀分离出来,至少需要加1.6mol/L的氢氧化钠溶液的体积是( )
| A、3.2L |
| B、2 L |
| C、1.8 L |
| D、1.5 L |
下列各组微粒中,互为同位素的是( )
| A、40Ca和40Ar |
| B、H2O和H2O2 |
| C、O2和O3 |
| D、H、D、T |
下列轨道表示式能表示磷原子的最低能量状态的是( )
A、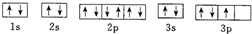 |
B、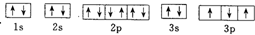 |
C、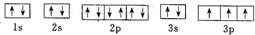 |
D、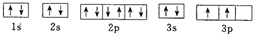 |
向饱和澄清石灰水中加入少量CaC2,充分反应后恢复到原来的温度,所得溶液中( )
| A、c(Ca2+)、c(OH-)均增大 |
| B、c(Ca2+)、c(OH-)均保持不变 |
| C、c(Ca2+)、c(OH-)均减小 |
| D、c(OH-)增大、c(H+)减小 |
下列物质分类正确的是( )
| A、SO2、SiO2、CO2、CO均为酸性氧化物 |
| B、稀豆浆、硅酸、水玻璃、氯化铁溶液均为胶体 |
| C、烧碱、冰醋酸、四氯化碳、NH3均为电解质 |
| D、BaSO4的水溶液不导电,但BaSO4是强电解质 |