题目内容
下列物质分类正确的是( )
| A、SO2、SiO2、CO2、CO均为酸性氧化物 |
| B、稀豆浆、硅酸、水玻璃、氯化铁溶液均为胶体 |
| C、烧碱、冰醋酸、四氯化碳、NH3均为电解质 |
| D、BaSO4的水溶液不导电,但BaSO4是强电解质 |
考点:酸、碱、盐、氧化物的概念及其相互联系,电解质与非电解质
专题:物质的分类专题
分析:A.酸性氧化物的概念是和碱反应生成盐和水的氧化物;
B.根据胶体、溶液等的定义和常见物质判断;
C.根据电解质和非电解质的概念判断;
D.硫酸钡是难溶的盐,熔融状态完全电离.
B.根据胶体、溶液等的定义和常见物质判断;
C.根据电解质和非电解质的概念判断;
D.硫酸钡是难溶的盐,熔融状态完全电离.
解答:
解:A.SO2、SiO2、CO2都可以与碱反应生成盐和水,属于酸性氧化物,CO不能与碱反应是不成盐氧化物,故A错误;
B.豆浆是胶体,硅酸、水玻璃、氯化铁溶液不是胶体,故B错误;
C.烧碱、冰醋酸在水溶液里或熔融状态下能导电,是电解质,四氯化碳、NH3均为非电解质,故C错误;
D.硫酸钡是难溶的盐,熔融状态完全电离;所以BaSO4是强电解质,故D正确;
故选D.
B.豆浆是胶体,硅酸、水玻璃、氯化铁溶液不是胶体,故B错误;
C.烧碱、冰醋酸在水溶液里或熔融状态下能导电,是电解质,四氯化碳、NH3均为非电解质,故C错误;
D.硫酸钡是难溶的盐,熔融状态完全电离;所以BaSO4是强电解质,故D正确;
故选D.
点评:本题考查混合物、电解质、非电解质、氧化物的分类等概念,题目较为简单,学习中注意对概念的理解要准确.

练习册系列答案
相关题目
下列说法中,正确的是( )
| A、元素周期表中的第ⅠA族元素全部是碱金属元素 |
| B、元素周期表中的第ⅦA族元素全部是非金属元素 |
| C、元素周期表中的0族元素最外层电子数都是8个 |
| D、元素周期表划分为7个周期18个族 |
下列物理变化过程中,化学键被破坏的是( )
| A、碘升华 |
| B、冰融化成水 |
| C、蔗糖溶于水 |
| D、氯化钠晶体在熔化状态下电离 |
已知H2(g)+
O2(g)=H2O(g);△H=-241.8kJ/mol.下列说法中不正确的是( )
| 1 |
| 2 |
| A、H2的燃烧热为-241.8kJ |
| B、2H2(g)+O2(g)=2H2O(g);△H=-483.6kJ/mol |
| C、1molH2完全燃烧生成液态水放出的热量大于241.8kJ |
| D、断开1molH2O的化学键吸收的总能量大于断裂1molH2和0.5 molO2的化学键所吸收的总能量 |
下列物质不能通过单质之间直接化合得到的是( )
| A、NaCl |
| B、Na2O2 |
| C、AlCl3 |
| D、FeCl2 |
下列溶液中的氯离子的物质的量浓度与50mL 1mol?L-1的AlCl3溶液中氯离子物质的量浓度相等的是( )
| A、25mL 3 mol?L-1的KCl |
| B、75 mL 1.5 mol?L-1的CaCl2 |
| C、150 mL 1 mol?L-1的NaCl |
| D、100 mL 2 mol?L-1的FeCl3 |
下列反应△H<0的是( )
A、、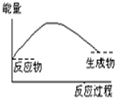 |
B、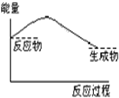 |
C、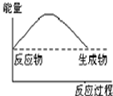 |
D、、 |
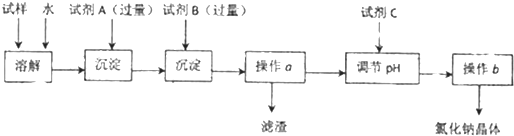
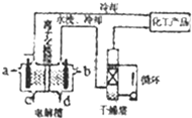 工业上电解饱和食盐水能制取多种化工原料,其设备示意图如图:
工业上电解饱和食盐水能制取多种化工原料,其设备示意图如图: