��Ŀ����
3��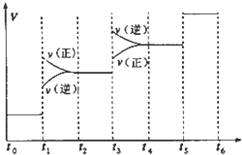 �����Ǻϳɰ�����Ҫԭ�ϣ��ϳɰ���Ӧ���Ȼ�����ʽ���£�
�����Ǻϳɰ�����Ҫԭ�ϣ��ϳɰ���Ӧ���Ȼ�����ʽ���£�N2��g��+3H2��g��?2NH3��g������H=-92.4kJ•mol-1
���ϳɰ���Ӧ�ﵽƽ��ı�ijһ������������ı�N2��H2��NH3����������Ӧ������ʱ��Ĺ�ϵ��ͼ��ʾ������˵����ȷ���ǣ�������
| A�� | ͼ��t1ʱ����ƽ���ƶ������������������¶� | |
| B�� | ��ʾƽ��������NH3�ĺ�����ߵ�һ��ʱ����t5��t6 | |
| C�� | �¶�ΪT��ʱ����2amolH2��amolN2����0.5L�ܱ������У���ַ�Ӧ����N2��ת����Ϊ50%����Ӧ��ƽ�ⳣ��Ϊ$\frac{16}{{a}_{2}}$ | |
| D�� | ��t2��t3ʱ��Σ���������������䣬����һ�����Ķ������壬N2��Ũ�Ȳ��� |
���� A���ɷ�Ӧ������ʱ��Ĺ�ϵͼ���֪��t1ʱ���淴Ӧ���ʶ�����ƽ�������ƶ�������ƽ���ƶ�����������������ѹǿ��
B��t3ʱ�����淴Ӧ���ʾ�Ѹ��������ƽ��������У��������İٷֺ����Ǽ�С�ģ�����ʾƽ��������NH3�ĺ�����ߵ�һ��ʱ����t2-t3��
C��N2��g��+3H2��g��?2NH2��g��
��ʼ 2amol/L 4amol/L 0
��Ӧ amol/L 3amol/L 2amol/L
ƽ�� amol/L amol/L 2amol/L
���ݻ�ѧƽ�ⳣ������ʽ���м��㣻
D����t2��t3ʱ��Σ���������������䣬����һ�����Ķ������壬����ֵ�Ũ�Ȳ��䣬ƽ�ⲻ�ƶ���
��� �⣺A���ɷ�Ӧ������ʱ��Ĺ�ϵͼ���֪��t1ʱ���淴Ӧ���ʶ�����ƽ�������ƶ�������ƽ���ƶ�����������������ѹǿ�������������¶ȣ���A����
B��t3ʱ�����淴Ӧ���ʾ�Ѹ��������ƽ��������У��������İٷֺ����Ǽ�С�ģ�����ʾƽ��������NH3�ĺ�����ߵ�һ��ʱ����t2-t3��������t5��t6����B����
C��N2��g��+3H2��g��?2NH2��g��
��ʼ 2amol/L 4amol/L 0
��Ӧ amol/L 3amol/L 2amol/L
ƽ�� amol/L amol/L 2amol/L
���Ի�ѧƽ�ⳣ��K=$\frac{��2amol/L��^{2}}{��amol/L������amol/L��^{3}}$=$\frac{4}{{a}^{2}}$��L/mol��2����C����
D����t2��t3ʱ��Σ���������������䣬����һ�����Ķ������壬����ֵ�Ũ�Ȳ��䣬ƽ�ⲻ�ƶ������Ե�����Ũ�Ȳ��䣬��D��ȷ��
��ѡD��
���� ���⿼����Ӱ�컯ѧ��Ӧ���ʵ����ء�ͼ���������ѧƽ������ʽ�����֪ʶ�㣬ע��֪ʶ��Ǩ�ƺ�Ӧ���ǹؼ����ѶȲ���

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�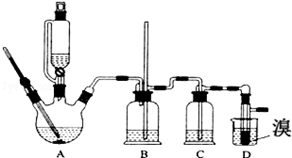
�й������б����£�
| �Ҵ� | 1��2-�������� | ���� | |
| ״̬ | ��ɫҺ�� | ��ɫҺ�� | ��ɫҺ�� |
| �ܶ�/g•cm-3 | 0.79 | 2.2 | 0.71 |
| �е�/�� | 78.5 | 132 | 34.6 |
| �۵�/�� | һl30 | 9 | -1l6 |
��1��д��װ��A�еķ�Ӧ����ʽΪ��C2H5OH$��_{170��}^{Ũ����}$CH2=CH2��+H2O��
��2���ڴ��Ʊ�ʵ���У�Ҫ������Ѹ�ٵذѷ�Ӧ�¶���ߵ�170�����ң�������ҪĿ���Ǽ��ٸ������������ɣ�ͬʱ��װ��C��Ӧ����NaOH��Һ����Ŀ�������շ�Ӧ�п������ɵ��������壮
��3����1��2-��������ֲ�Ʒ���ڷ�Һ©���м�ˮ�����ã�����Ӧ���²㣨��ϡ������¡�������������������δ��Ӧ��Br2������NaOH��Һϴ�ӳ�ȥ��
��4����Ӧ������Ӧ����ˮ��ȴװ��D�����ֲ��ܹ�����ȴ�����ñ�ˮ������ԭ��������ñ�ˮ��ȴ��ʹ��Ʒ���̶��������ܣ�
ijѧ��Ϊ��̽����ˮ�ijɷ֣���������һ�����̽�����̣�����дʵ�鱨�森
| ʵ�鲽�� | �������� | ʵ������ | ���ۻ���� |
| 1 | �۲���ˮ����ɫ | ����Cl2 | |
| 2 | ����ɫ������� | ����H+ | |
| 3 | ȡ������ˮ���Թ��У�����ϡ�����ữ����������Һ | �а�ɫ�������� | |
| 4 | ȡ������ˮ���Թ��У������ɫ���� |
| A�� | c��NH4+����c��Cl-����c��OH-����c�� H+�� | B�� | c��Cl-����c��NH4+����c�� H+����c��OH-�� | ||
| C�� | c��NH4+��+c�� NH3��=c��Cl-��+c��OH-�� | D�� | c��NH4+��+c�� NH3•H2O��+c�� NH3��=c��Cl-�� |
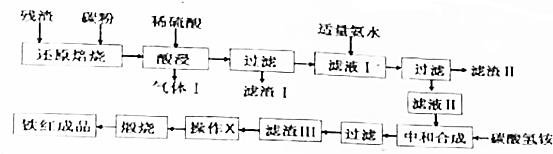
�������ϣ�
�ֽ������ӷ���������pH��
| �������� | Fe3+ | Al3+ | Fe2+ |
| ��ʼ������pH | 2.2 | 3.1 | 7.5 |
| ��ȫ������pH | 3.5 | 5.4 | 9.5 |
��������Ϲ������̼��ṩ����Ϣ���ش��������⣺
��1����������Ҫ�ɷ�ΪH2���ѧʽ����ͬ�������������Ҫ�ɷ�ΪAl��OH��3��Fe��OH��3��
��2������XΪϴ�ӣ���������ƣ���
��3������Һ���м���������ˮ����Ŀ���ǵ�����Һ��pH��5.4��7.5֮�䣮
��4���ڡ�����������У����ڿ����С������ʱ���������Һ��Fe2+�������½�����ԭ���ǣ������ӷ���ʽ��ʾ����4Fe2++O2+4H+�T4Fe3++2H2O��
��5��Ϊ�ⶨ��Һ���е�Fe2+�ĺ�����ʵ�����г������Ը��������Һ���еζ����÷�Ӧ�����ӷ���ʽΪ��MnO4-+5Fe2++8H+�TMn2++5Fe3++4H2O��ȡ20.00mL��Һ������ƿ�У���0.1mol/L���Ը��������Һ�ζ����յ�ʱ�����˱����Ը��������Һ12.00mL������Һ����c��Fe2+��=0.3mol/L��

��֪25��ʱ����������������������ʽ��ȫ����ʱ��Һ��pH���±���
| ������ | Zr��OH��4 | Fe��OH��3 | Al��OH��3 | Fe��OH��2 |
| ��ʼ����ʱpH | 1.2 | 2.7 | 3.4 | 6.3 |
| ��ȫ����ʱpH | 2.4 | 3.2 | 5.2 | 9.7 |
ZrSiO4+4NaOH�TNa2ZrO3+Na2SiO3+2H2O
��2��Ϊ����߽����ʿɲ�ȡ�ķ�����ԭ�Ϸ�������Ӵ���������Ȼ������ν�ȡ���о����֣�
��3����������2�ijɷ�H2SiO3��H4SiO4���û�ѧʽ��ʾ��
��4���ð�ˮ����Һ2��pH����2.4��pH��3.4��Ŀ����ʹZr4+��ȫת��ΪZr��OH��4������ͬʱ��֤Al3+���ᱻ����������
��5��������������1�м���������Һ�����˲�������ٽ���Һ�ڲ���ͨ��HCl����������ͬʱ����Ũ������ȴ�ᾧ�����ˣ��ɻ��յõ������Ȼ���FeCl3���壮
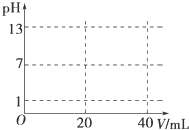 ��Һ�еĻ�ѧ��Ӧ��������ӷ�Ӧ������Ҫ��ش��������⣮
��Һ�еĻ�ѧ��Ӧ��������ӷ�Ӧ������Ҫ��ش��������⣮