题目内容
10.己知下列反应的离子方程式:a.向NaHCO3溶液中滴加稀盐酸:HCO3-+H+=CO2↑+H2O
b.向NH4Cl溶液中滴加NaOH稀溶液:NH4++OH-=NH3•H2O
下列说法正确的是( )
| A. | NaHCO3在水溶液中的电离方程式为NaHCO3=Na++H++CO32- | |
| B. | NaHCO3溶液与NaOH溶液反应的离子方程式为H++OH-=H2O | |
| C. | NH4NO3溶液与NaOH稀溶液反应的离子方程式为NH4++OH-=NH3•H2O | |
| D. | NH4NO3溶液与足量Ba(OH)2溶液反应的离子方程式为Ba2++CO32-=BaCO3↓ |
分析 A.碳酸氢钠电离出钠离子和碳酸氢根离子,碳酸氢根离子不能拆开;
B.碳酸氢根离子不能拆开,应该保留整体形式;
C.硝酸铵与氢氧化钠溶液反应生成一水合氨和硝酸钠;
D.硝酸铵与氢氧化钡溶液反应生成硝酸钡和一水合氨.
解答 解:A.NaHCO3在水溶液中电离出钠离子和碳酸氢根离子,正确的电离方程式为:NaHCO3=Na++HCO3-,故A错误;
B.NaHCO3溶液与NaOH溶液反应生成碳酸钠和水,正确的离子方程式为:HCO3-+OH-=H2O+CO32-,故B错误;
C.NH4NO3溶液与NaOH稀溶液反应生成硝酸钠和一水合氨,反应的离子方程式为:NH4++OH-=NH3•H2O,故C正确;
D.NH4NO3溶液与足量Ba(OH)2溶液反应生成硝酸钡和一水合氨,正确的离子方程式为:NH4++OH-=NH3•H2O,故D错误;
故选C.
点评 本题考查了离子方程式的判断,为高考的高频题,题目难度不大,注意掌握离子方程式的书写原则,明确离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合原化学方程式等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
20.下列有关描述不正确的是( )
| A. | 钠在空气和氯气中燃烧,火焰皆呈黄色,但生成固体颜色不同 | |
| B. | 新制饱和氯水和浓硝酸光照下均会有气体产生,其成分中都有氧气 | |
| C. | 浓硫酸具有较强酸性,能使Cu转化为Cu2+ | |
| D. | 灼烧NaOH固体时不能使用瓷坩埚,因为坩埚中的SiO2能与NaOH反应 |
1.某品牌茶叶中铁元素的检验可经过以下四个步骤完成:将茶叶灼烧灰化→用浓硝酸溶解茶叶灰→过滤得到的滤液→检验滤液中的Fe3+.图是该实验可能用到的实验用品.有关该实验的说法中错误的是( )


| A. | 第一步需选用仪器①、②和⑨,仪器①的名称叫坩埚 | |
| B. | 第二步用浓硝酸溶解茶叶灰,可能将Fe2+氧化成Fe3+ | |
| C. | 要完成第三步,需选用④、⑤和⑦,除夹持仪器外还缺滤纸 | |
| D. | 第四步,用试剂⑧检验滤液中的Fe3+,溶液中生成血红色沉淀 |
18.同温同压下,同物质的量的CH4气体与CO体积比是( )
| A. | 3:1 | B. | 1:1 | C. | 1:3 | D. | 2:3 |
15.下列各组试剂中.能用如图所示实验装置进行配备和收集气体的一组是( )
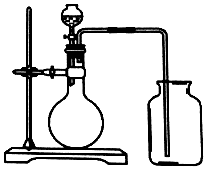

| A. | 锌和稀硫酸 | B. | 碳酸钙和硫酸 | ||
| C. | 过氧化氢和二氧化锰 | D. | 硫酸铵和氢氧化钠 |
2.物质的量为0.10mol的镁条在足量的、且只含有CO2和O2混合气体的容器中充分燃烧(产物不含碳酸镁),反应后容器内固体物质的质量可能( )
| A. | 2.2g | B. | 4.2g | C. | 4.4g | D. | 4.8g |
19.下列叙述正确的是( )
| A. | 强电解质都易溶于水,所以BaSO4是弱电解质 | |
| B. | 氨气的水溶液可以导电,但氨气属于非电解质 | |
| C. | 使用催化剂可以让不自发的化学反应自发进行 | |
| D. | 电解质溶液的导电过程属于物理变化 |
20.我国古代劳动人民的发明创造,为世界文明的发展作出巨大贡献,下列说法不正确的是( )
| A. | 活字印刷的泥活字是硅酸盐材料制成的 | |
| B. | 制指南针的磁石主要成分是四氧化三铁 | |
| C. | 引爆黑火药后,硫磺燃烧生成三氧化硫 | |
| D. | 用树皮造纸过程主要是提取其中的纤维素 |